В открытом сосуде 2

- Главная
- Вопросы & Ответы
- Вопрос 17050294
Главный Попко
более месяца назад
Просмотров : 9
Ответов : 1
Лучший ответ:
Суррикат Мими
Задание решить невозможно, оно недоопределено, а именно, не указан размер сосудов, их взаимное расположение, количество жидкости в каждом, гду у них отверстия и т.п. Поэтому если нет описания словами, хотя бы нарисуй схематично. От этого зависит правильный ответ.
более месяца назад
Ваш ответ:
Комментарий должен быть минимум 20 символов
Чтобы получить баллы за ответ войди на сайт

Лучшее из галереи за : неделю месяц все время































Другие вопросы:
Пармезан Черница
ответьте на вопросики пожалуйста) 1)что такое лес? 2)Есть такое выражение “предписанное выжигание”Что это означает? 3)В каком веке начали активно распространяться лесные пожары? 4)Увеличивается ли ежегодно число пожаров ? 5)Кто главный виновник пожаров? 6)От чего может произойти возгорание леса? 7)К…
более месяца назад
Смотреть ответ
Просмотров : 1
Ответов : 1
Главный Попко
в клетках растения 6 хромосом(2n). сколько хромосом содержат: а)яйцеклетка г)клетки зародыша б)спермий д)клетки эндосперма в)зигота е)материнская клетка пыльцы
более месяца назад
Смотреть ответ
Просмотров : 1
Ответов : 1
Васян Коваль
велосипедист и мотоциклист выехали одновременно из одного пункта В одном направлении скорость мотоцикла 40 км ч а велосипедиста 12 км ч Какова скорость их удаления друг от друга через несколько часов расстояние между ними будет 56 км
более месяца назад
Смотреть ответ
Просмотров : 3
Ответов : 1
Мари Умняшка
как украсить вечный террариум неиспользуя мох. и может ли он ( террариум) обойтись без мха
более месяца назад
Смотреть ответ
Просмотров : 3
Ответов : 1
Зачетный Опарыш
Два учащихся спорят:один утверждает,что кочан капусты-это гигантская вегетативная почка,а другой-это генеративная почка.Кто из них прав?Почему?
более месяца назад
Смотреть ответ
Просмотров : 2
Ответов : 1
Источник
5.4. Практическое применение уравнения состояния идеального газа
5.4.1. Уравнение состояния для идеального газа в открытом сосуде
При рассмотрении идеального газа, находящегося в открытом сосуде, необходимо учитывать, что вследствие изменения термодинамических параметров часть газа выходит из сосуда. При этом уравнение состояния записывается только для той части газа, которая остается в сосуде.
Для идеального газа, находящегося в открытом сосуде, необходимо учитывать следующее:
- масса газа изменяется в результате изменения его термодинамических параметров:
m ≠ const;
- рассматривается газ, оставшийся в сосуде определенного объема, т.е. объем газа фиксирован:
V = const;
- давление газа может изменяться или оставаться постоянным (в зависимости от условия задачи), причем на изменение давления в условии задачи обычно бывает четкое указание.
Если давление идеального газа в открытом сосуде по условию задачи изменяется (p ≠ const), то уравнение Менделеева — Клапейрона записывается для двух состояний газа в виде системы (рис. 5.7):Рис. 5.7
p1V=m1MRT1,p2V=m2MRT2,}
где p
1, m
1, T
1 — давление, масса и температура газа в начальном состоянии; p
2, m
2, T
2 — указанные параметры газа в конечном состоянии; V — объем сосуда; M — молярная масса газа; R — универсальная газовая постоянная, R ≈ 8,31 Дж/(моль ⋅ К).
Если давление идеального газа в открытом сосуде по условию задачи остается постоянным (p = const), то изменения некоторых характеристик газа в открытом сосуде можно вычислить по следующим формулам:
- изменение массы
Δm=m1−m2=m1(1−T1T2),
где m
1 — первоначальная масса газа; m
2 — масса газа в конце процесса; T
1 — термодинамическая (абсолютная) температура газа в начале процесса; T
2 — термодинамическая (абсолютная) температура газа в конце процесса;
- изменение плотности
Δρ=ρ1−ρ2=ρ1(1−T1T2),
где ρ1 — первоначальная плотность газа; ρ2 — плотность газа в конце процесса;
- изменение количества вещества
Δν=ν1−ν2=ν1(1−T1T2),
где ν1 — первоначальное количество вещества (газа) в сосуде; ν2 — количество вещества (газа) в сосуде в конце процесса.
Пример 11. В открытом сосуде объемом 450 дм3 содержится некоторое количество идеального газа. Температуру газа увеличивают от 27 до 177 °С. Давление газа остается постоянным и равным 166 кПа. Сколько моль газа выйдет из сосуда?
Решение. Запишем уравнение Менделеева — Клапейрона для двух состояний газа, находящегося в открытом сосуде, при нагревании:
- для начального состояния
pV = ν1RT
1;
- для конечного состояния
pV = ν2RT
2;
где p — давление газа, p = const; V — объем газа (сосуда), V = const; ν1, ν2 — количество вещества (газа) в начале и в конце процесса; R — универсальная газовая постоянная, R = 8,31 Дж/(моль ⋅ К); T
1, T
2 — температура газа в начале и в конце процесса.
Первое уравнение позволяет получить формулу для расчета количества вещества (газа) в начале процесса:
ν1=pVRT1.
Подстановка полученной формулы в уравнение
Δν=ν1(1−T1T2)
дает искомую разность
Δν=pVRT1(1−T1T2)=pV(T2−T1)RT1T2.
Для вычисления искомой величины необходимо перевести температуру из градусов Цельсия в кельвины:
T
1 = t
1 + 273 = 27 + 273 = 300 К,
T
2 = t
2 + 273 = 177 + 273 = 450 К.
Произведем вычисление:
Δν=166⋅103⋅450⋅10−3(450−300)8,31⋅450⋅300=10 моль.
При нагревании из сосуда вышло 10 моль газа.
Пример 12. В баллоне при температуре 15 °С находится идеальный газ. Из баллона выходит 40 % газа, а температура при этом понижается на 8,0 °С. Во сколько раз уменьшится давление газа в баллоне?
Решение. Запишем уравнение Менделеева — Клапейрона для двух состояний газа, находящегося в открытом сосуде:
- для начального состояния
p
1V = ν1RT
1;
- для конечного состояния
p
2V = ν2RT
2;
где p
1 — давление газа в начальном состоянии; p
2 — давление газа в конечном состоянии; V — объем газа (сосуда), V = const; ν1, ν2 — количество вещества (газа) в начале и в конце процесса соответственно; R — универсальная газовая постоянная, R = 8,31 Дж/(моль ⋅ К); T
1, T
2 — температура газа в начале и в конце процесса соответственно.
Искомой величиной является отношение давлений p
1/p
2, которое определим из отношения уравнений:
p1Vp2V=ν1RT1ν2RT2, т.е. p1p2=ν1T1ν2T2.
В результате процесса из баллона выходит 40 % газа, поэтому количество вещества (газа) ν2, оставшегося в баллоне, составляет 60 % от количества вещества (газа) ν1, которое было в начале процесса:
ν2 = 0,6ν1.
Для вычисления искомой величины необходимо сделать перевод температуры, заданной в градусах Цельсия, в кельвины:
T
1 = t
1 + 273 = 15 + 273 = 288 К,
T
2 = t
2 + 273 = (t
1 − Δt) + 273 = (15 − 8,0) + 273 = 280 К.
Подстановка температур и количества вещества (газа), оставшегося в баллоне, в выражение для искомой величины дает
p1p2=ν1T10,6ν1T2=T10,6T2=2880,6⋅280=1,7.
Давление газа в баллоне понизится в 1,7 раза.
Источник


Похожие вопросы:

Физика, 07.03.2019 20:00
1. определите объём стальной плиты, полностью погруженной воду, если на нее действует выталкивающая сила 35 н 2. вычислите архимедову силу, действующую на брусок размером 2на 10 на 4 см, если он наполовину погружен в
спирт. 3.какую силу необходимо приложить к плите массой 4 т при её подъеме со дна водоема, если объем плиты 2 м в кубе.
Ответов: 2

Физика, 08.03.2019 13:30
Тело объёмом 5 дм имеет массу 5 кг. утонет ли это тело в керосине? с решением.
Ответов: 4

Физика, 09.03.2019 04:30
Электрон движется в однородном магнитном поле по окружности, радиус kоторой r=2мм емли модуль импульса электрона p=6.4 *10^-23, то модуль индукции b магнитного поля равен?
Ответов: 2

Физика, 09.03.2019 12:10
Медная проволока длинной 15 м и площадью поперечного сечения 2,5мм в квадрате включена в цепь аккумулятора .сила тока в цепи 0,5а. определить напряжение н полюсах аккумулятора.
Ответов: 4

Физика, 10.03.2019 20:29
Какую скорость будет иметь камень массой 4 кг в конце падения с высоты 36 м, если в течение всего полёта действовала сила сопротивления воздуха, равная 4 н
Ответов: 3

Физика, 11.03.2019 13:00
Определить число атомов, содержащихся в 1 г гелия; в 1 г полностью диссоциированного азота; в 1 м3 аргона при нормальных условиях
Ответов: 2

Физика, 12.03.2019 13:05
Электрон разгоняется однородным полем на участке 10-2 см до скорости 4106 м/с. найти: 1) работу поля; 2) разность потенциалов на концах участка
Ответов: 2

Физика, 13.03.2019 15:00
Уравнение движения тела задано: x=-200+16t-1,5t(в квадрате). описать из какой точки, в каком направлении, с какой начальной скоростью, с каким ускорением происходит движения и каким оно является?
Ответов: 1

Физика, 14.03.2019 20:02
Нужно решить две 1. дано: s дна кострюли – 1300 см² найти: p кастрюли на стол, если в ней налито три целых, девять десятых литра воды. 2. дано: p на входе в метро = 101 целая, три десятых килопаскаль. p на платформе внизу = 101674 паскаль. найти: h метро
Ответов: 3

Физика, 15.03.2019 22:00
1)порівняйте силу струму в лампі розжарення в момент вмикання її в мережу і силу струму робочу її режимі 1. у момент вмикання менша 3.однакові 2. у момент вмикання більша 4.у момент вмикання може бути різна 2)у скільки разів зміниться загальна сила струму у двох однакових спіралях електричних плиток, якщо переключити їх з паралельно на послідовне з’єднання при незмінній напрузі в мережі 1.зменшиться в 2 рази 3.не зміниться 2.зменшиться в 4 рази 4.зменшиться у 8 разів
Ответов: 3

Физика, 17.03.2019 23:20
Вкаком положении поршня в начале или конце такта сжатия величина внутренней энергии и т-ра газа в цилиндре двигателя внутреннего сгорания больше? объясните за счет чего произошли эти изменения
Ответов: 2

Физика, 18.03.2019 01:40
Определите ускорение конца секундной стрелки часов если он находиться на расстоянии r=2 см(длина l окружности радиуса r определяется по формуле l=6,28r)
Ответов: 2
У тебя есть свой ответ?
5. в открытом сосуде 1 и закрытом сосуде 2 находится вода. если открыть кран к, то: 1) вода обязате…
Отправлено
Вопросы по другим предметам:

Литература, 26.04.2020 19:36

Українська мова, 26.04.2020 19:35

Литература, 26.04.2020 19:36

Другие предметы, 26.04.2020 19:36

Литература, 26.04.2020 19:36

Українська література, 26.04.2020 19:36

Математика, 26.04.2020 19:36

История, 26.04.2020 19:36


Литература, 26.04.2020 19:36
У тебя есть свой ответ?
5. в открытом сосуде 1 и закрытом сосуде 2 находится вода. если открыть кран к, то: 1) вода обязате…
Отправлено
Источник
1. Вспоминай формулы по каждой теме
2. Решай новые задачи каждый день
3. Вдумчиво разбирай решения
Три одинаковых сосуда, содержащих разреженный газ, соединены друг с другом трубками малого диаметра: первый сосуд — со вторым, второй — с третьим. Первоначально давление газа в сосудах было равно соответственно (р, 3р) и (р). В ходе опыта сначала открыли и закрыли кран, соединяющий второй и третий сосуды, а затем открыли и закрыли кран, соединяющий первый сосуд со вторым. Как изменилось в итоге (уменьшилось, увеличилось или осталось неизменным) количество газа в первом сосуде? (Температура газа оставалась в течение всего опыта неизменной.)
1) При первой открывании и закрывании кранов, в соответствии законам Дальтона и Бойля-Мариотта, установившееся давление во втором и третьем сосудах будет [dfrac{3p}{2}+dfrac{p}{2}=2p] 2) При втором открывании и закрывании, с учетом тех же законов, установившееся давление в первом и втором будет равно [dfrac{2p}{2}+dfrac{p}{2}=1,5p] 3) Так как объем сосуда не изменился, а температура по условию постоянна, то в соответствии закону Клайперона – Менделеева [pV=nu R T Rightarrow nu=dfrac{pV}{RT}] Знаменатель остался прежним, а числитель увеличился, значит и количество газа увеличилось.
Ответ:
Сжиженные газы с низкими температурами кипения хранят в открытых теплоизолированных резервуарах при нормальном давлении, с контактом с атмосферой. При таком хранении потери на испарение, отнесённые к единице массы сжиженного газа, уменьшаются при увеличении объёма сосуда. Объясните причины вышеизложенного, основываясь на известных физических законах и закономерностях.
1) Даже при хорошей теплоизоляции невозможно устранить полностью подвод тепла к сжиженным газам, значит, будет некоторое испарение вещества, потому что температура кипения таких газов ниже температуры атмосферы и существует теплопроводность.
2) Так как существует испарение, то в закрытых сосудах будет повышаться давление, что приведет к взрыву, поэтому газ хранят в открытых сосудах.
3) Подвод тепла к газу через стенки сосуда пропорционален площади стенок сосуда, а его масса пропорциональна объему. Объем же в свою очередь пропорционален кубу размеров сосуда. Поэтому с увеличением объема уменьшается испарение на единицу массы.
Ответ:
Чтобы вода в резервуаре быстрее закипела, источник тепла всегда помещают внизу. Желая охладить кастрюлю с горячей водой как можно быстрее, кастрюлю поставили на лёд. Является ли такой способ эффективным? Ответ поясните, указав какие физические явления и закономерности вы использовали для объяснения.
Нет, неверно.
Нагреватель ставится внизу, потому что нагретые слои воды, как более легкие, поднимаются вверх и таким образом достигается наиболее эффективное перемешивание и нагревание всей воды (по такому же принципу работает батарея в комнате). При охлаждении же дело происходит как раз наоборот: более холодные слои воды, как более тяжелые, опускаются вниз. Поэтому если поместить холодильник внизу, то перемешивания не будет, и остывание будет идти очень долго. Для более быстрого охлаждения надо поместить лед сверху.
Ответ:
На рисунке изображены графики двух процессов, проведённых с идеальным газом при одном и том же давлении. Графики процессов представлены на рисунке. Почему изобара (I) лежит выше изобары (II)? Ответ поясните, указав, какие физические закономерности Вы использовали для объяснения. 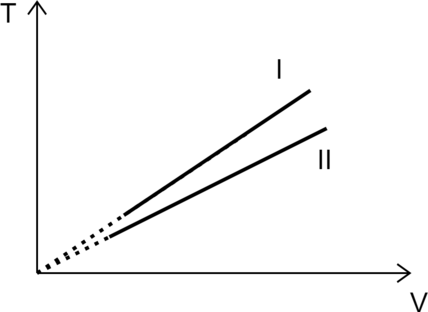
1. Идеальный газ подчиняется закону Клапейрона–Менделеева: [pV=nu R T,] где (p) – давление газа, (V) – объем, (nu) – количество газа, (T) – температура газа в Кельвинах.
Выразим температуру [T=dfrac{pV}{nu R}] 2. Зафиксируем объем (V_0), при этом отношение температур равно [dfrac{T_I}{T_{II}}=dfrac{dfrac{pV_0}{nu_I R}}{dfrac{pV_0}{nu{II}R}}=dfrac{nu_{II}}{nu_{I}}>1] Значит количество газа во втором больше, чем количество газа в первом.
Ответ:
1 моль разреженного гелия участвует в циклическом процессе 1–2–3–4–1, график которого изображён на рисунке в координатах V–T, где V — объём газа, Т — абсолютная температура. Постройте график цикла в координатах p–V, где р — давление газа, V— объём газа. Опираясь на законы молекулярной физики и термодинамики, объясните построение графика. Определите, во сколько раз работа газа в процессе 2–3 больше модуля работы внешних сил в процессе 4–1. 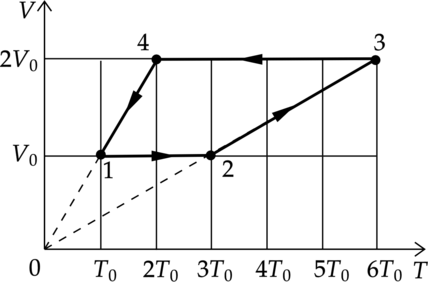
Проанализируем процессы:
1–2: Процесс изохорный, по закону Шарля (dfrac{p}{T}=const), температура увеличилась в 3 раза, значит и давление увеличилось в 3 раза.
2–3: Процесс изобарный, по закону Гей–Люсака (dfrac{V}{T}=const) и объем и температура увеличились в 2 раза.
3–4: В процессе 3–4 газ изохорно уменьшил свою абсолютную температуру и давление в 3 раза.
4–1: Газ вернулся в первоначальное состояние Перестроим график цикла в координатах p–V (см. рисунок). 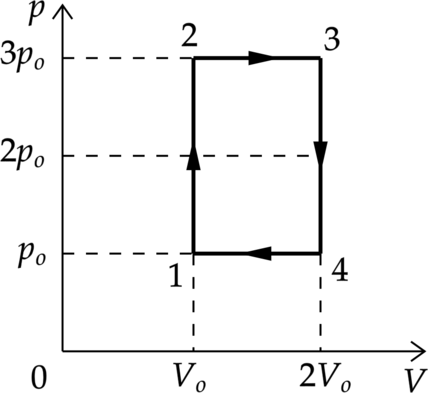
Работа газа в процессе 2–3 равна [A_{23}=pDelta V=3p_(2V_0-V_0)=3p_0V_0] Работа внешних сил в процессе 4–1 равна [|A_{41}|=pDelta V=p_0(2V_0-V_0)=p_0V_0] Значит работа газа в процессе 2–3 в 3 раза больше работы внешних сил в процессе 4–1.
Ответ:
На рисунке 1 приведена зависимость внутренней энергии (U) 2 моль идеального одноатомного газа от его давления p в процессе 1–2–3. Постройте график этого процесса на рисунке 2 в переменных (p—V). Точка, соответствующая состоянию 1, уже отмечена на этом рисунке. Построение объясните, опираясь на законы молекулярной физики. 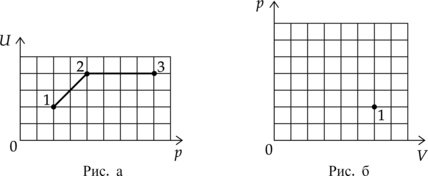
1. Проанализируем процессы:
1–2: Внутренняя энергия прямо пропорциональна температуре газа (U=dfrac{3}{2}nu R T ), значит в процессе 1–2 температура увеличивается, давление тоже увеличивается (по графику ). По основному газовому закону (dfrac{pV}{T}=const) объем будет постоянен. График будет представлять собой вертикальную прямую
2–3: В процессе 2–3 внутренняя энергия газа постоянна, а значит и температура постоянна (по пункту 1), давление увеличивается, значит, по основному газовому закону объем будет уменьшаться. График будет представлять гиперболу.
2. Построим график

Ответ:
На графике представлена зависимость давления неизменной массы идеального газа от его плотности. Опишите, как изменяются в зависимости от плотности температура и объём газа в процессах 1–2 и 2–3. 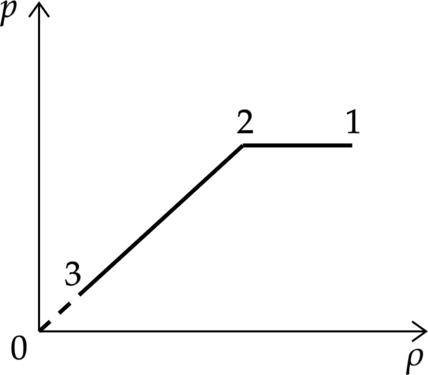
1. Плотность находится по формуле: [rho=dfrac{m}{V} quad (1)] тогда уравнение Клайперона–Менделеева можно переписать в виде [pV=dfrac{m}{mu}RT Rightarrow p=dfrac{rho}{mu}RT, quad (2)] где (m) – масса газа, (V) – его объем, (T) – температура газа. 2. Процесс 1–2.
Плотность уменьшается при постоянном, в соответствии с формулой (1) объем будет увеличиваться, а температура будет увеличиваться в соответствии с формулой (2).
Процесс 2–3.
Плотность уменьшается вместе с давлением, причем давление уменьшается пропорционально плотности (p sim rho), а это означает, что температура газа постоянна, а по формуле (1) объем увеличивается.
Ответ:
Источник
