В сосуде находится смесь гелия и неона молярная масса
Ç^´®pPÂpLú>î@mIr^%iºÅ$!}Üd/.B/:±ÄÍè¦pIQó ?A²ÀõLÈ«¨ ÇÎqæé¢I^©ËäÎÉöBºNÆ/¼KÿQIâ¥#Áø¨6=lÓ×ßáöè¼ Io¿W’|¯ZµO7FÀ¨üI>Q]#U.UÒÅïÕíÀ*Í4DND,¤6Þ§
Ú»
ðKR> cÒtIfÔ
qoOuOÐeÁ»yF)§ët©PezA¤xü×ØJ/£¢BÄKÃK$°®ôc½ÖÉû ¢C@%G0-ÙAôAE©%7£?ÊåBFÙ´¨hëÉý|ÀÏn ýò_ð
ôú®ãuªwbÂL|>Ù¶RÝüñÊ#æÁï(ÐMô@i´×ÀtaIìÄA&X>àirX}H]pqªtû%”µô¨A=¢àLOÒÀ#$n&^F-³àb5D=kðá1 TÉÜ¢¿ÿEöG$¥w^Éàc”»HС2
©? É?BÒ1Î⣫²9T4nº¾¾ÄóuJ?øÕõE«õz
ðáoñGòéøxúOÒ½ËUÏé®÷ëCJ_zÊ¿Å`¬øC`7oUÓ# |ñ¾]Ì7e
Ö[Þ®Ë
[zæØ6kºÏXÀ±¯WÏ_0¯ñ÷ýÂLî#®?BÇÔ®¤dɹ(üJDYV¥¡æh¼éf¬[öÎ ¶«”®Â0Z×Gxèl Cã¢=;L²0ÔÕpÎÓÈ>Á̱-¤_nÄô’d(drYÁVªÄDÀµ!}è¢Gì>&83§JÁ+U¼ô-Dÿy`¬^´Í¼¨èõéßnè±âSIСY
ü¬æ¯ i«àXMĸ Ê×WâET;T´z£ü=³&åZõéYíå£Õ4lk%7Qµ³T®>~=·zBt¹oÙíºÍÑ(qNQ+6>¬ðxJ»øϲٹB^óÓÄ,ÀØÛUKzáT8ÒÅÑ$î~5M+(YHÚEEQ=,ÉÜë¡a¢:E£QL¥FƲ?L®{}P驨w”[/Ó¡|Y’EßDí=y#õ1´ (Iîé.3rߤ h#HÍ5ëj㸽jÇ~ÝàI&/RktZȲÕ%î þ®NqÚ¿Ôk¶(ú.k(
kh/p£«sJ% WSÓϧ¡^iúÜ
c6&íç*ð%{áÛj_¯3×+W”=ý°§¢¤u¤øY=HÁ ¸©WÖÔ¬¸·uιÏåy8é,Ï:Ü009´¼f×àåô¯:ðó¼qi¡Ë1
}j’p^ùíëð5lEÏ’s[:C&s£ /o[¶ÍæÛ)
í ~/qÀ¸ré7nkøÿ(`}0)EÚJÃÂöÁEÏV³(«Ï;7³ÐäkpÓU8älV_®60ÑrÿìùºS ¡èY?â§!8аyÁ¬Ï®>ÇÃ=ÕÙÑat±e;¥*Tæte¬¡S”ÚqÙ[9Î)c²ÒÛø¨e»+¢£Î Àg¸¹¾!ñgÓÒdý¥e1° Ýä;ÀymTJÆ’Xy¡°zÛBM÷¡¬U@ È.
Yº0¯ª~ígjsÜÙ
1JäÃ0ìTÌA/9EC&ÞGÁ+¬ºCcµ
6觵R-¬:pX+ÔH+%EçáíÓ4svÛ±L95s4S2pii¦+ì#ÀB-Çb0 îØÞ*¨2ÎÙÇzB@u*³:@*sEÑü¿r±£äæèÀ/Ðsç¹Z`¢ëð½pPëXcµØ®´¡)ܨ_¦ûGDOW@6T»ûTãnºäBµÁ÷ÌäÃ$+aÂÐÈó µÊ/]Q0©w#Ävà¹OϪsû)u6m³èbªùË68Íh~N7»à
OkCiêÕöÒÁýJo1N¨`éÞ#è¸Ë¾g`,t/m´+I©>ÜjØþINvã ÖÅó½6^¨a%;ür1·|»ÂÎëê&¹ïgyOx>s/.)g.ÑÜ/*f·åsdz?”²x½ÁÊ2>»fW¥îÊýTr^7S.Úª.âv
^îÖ6%
½9ûEön¥ÎWBÌ¡o~l)
«C^¯ã !?²j^Ê+¶d~åi})HçTdiçÔ”²¬;Ð Ü(e 1″Z,K¬B_Ê
Dåq Þ)¹ñ°å®·ÝÇòn7¨v
%ë eBØý¬ ¥CU¢RÒh:ûË]+ =©ÛTÛ¢âÔ]coV¶ë2ô1¥´Výz¯fV
BZ´_Äk¥òs˾ð6e¢ÀÒ£Z»5Ù÷òÒ ÁÓ}ëN@%ãâ+p·¶®L¢Ô[¬
ë&ús~³Ð¼Mý½.×-dä ôÒb FÙwàæ©Ù¿è²
vwí¿ÓsZ!¤à¶²bAè0ÙsNÌcîA¤¯Cë `=ä)óFG’5Y°GñJ åÎÌ[«,ÈË-þÌ&] ½`uj>½`»v@ühÆ ±»Ï²xu0(^èº=1{Ù=:óJ[½ýÂ5Øö+dËÍäá®Ü>êMriu}^,ToFø¬Lì/¤[luèGkÂN§Êpt,”lFv:$Ô°·¥H¿2Ùدè1KU¸Òk
¥:{÷æNöNÆÃ0X4®8ÔÜÎ[Nû|«ÚÒ0ï¬Ã£kÎêáxYôÈæ:@)ª¤¨Áñû¬Ùt@Y§uUriw£âÄaeÅïû77tVVÔGCŶÝÑz’¤SO$ý½ aÒÑZA-aèÒvÅ·Ò+ls½S´ÖöÏÜí/3ÍF]°´r!dU.ØOMïÚM±ðU¦ kY#2æõ¡Fâ·0JXÖZ×J4XjÍT÷×¾¶Søm{NÞ³´ì~¾©@ãĨ>Ýϧs¦%°?öjÞXÛËk®asù~#:¥vzbMrmÐä:ÌD¥Ù½çæ¶N´ìlØ>h]Þ)ç¤êȦ£M&ve_KU)E6kós¶ÆËouV%±÷ÖG^ sÝ»[÷ö%+¿3Qì×Øsiãm²Ý8áýjìy’+ÌnG5»ÒbÛkú!b¼_5ɾï´7J8ext×l8xàý¾ @uÏ28Öõ,ûmU¶Y5;èÈÛܼ)»2nÌÃÞDx#,d?[ËÙïowÑåÂC¤
ß²Ýh[_¢Õ{
)g±Vͦ½ùþ~RàÆ$áq:ÑæÞ_¾HjÊ£üÑN!µ^d3©ÊI¨aVQôÊý!O$wÊRsÜ0¹Øå9
C5a¬ÃØ
¡óÃ0¼ð£ÒfÒ£ª|8í>ECÈļ_÷ÄÇêê Edb¢Oãà,Ò0dY0Ù²FaȲFaȲa²eÂeIEhL_eö5ä`k·ÓpÎlþlZN³©¡ê§:@¤È}ªyÍ_ùÒç
Ö¤rÇ8»Ç57u7NÐ>QX´*æ,ÓËê
HÞý·MieQ4ê?ê3z®C¦.£>dÕvVJ|ò
Ôô9³ìWö¨GK]ß·Ù
h¶sUÄñÄså.µ9Ï~¯¯¼´bûêzåu}â£4%¹-gíæ¼²ÃB/cÌçÚ¥ES´m5ü_Ï7î{ª(»§×¸üÙ Ó/Ì^K=pXwÓK¤áï5É^j9Ãùãd¿,Ͽȯ®éhÊû;=¥&z@^¢¼¾(
:inÔ×Á×Ãe
8^Ómvàb£Â]yadÞØ1¨Å±CÄ-¬G~6ïªPYcÓ+
mö6m&ñ7L0eØÔ«K¨a]Qd¬Ã¿þÔzØ{D¬ÂPåjÊa¬ÂPåj+W4kª¶RíÕp*½ÑyìlNâÛP-XB ÌIRä>
gÙFI$sÉæ4
Cæ4
Cæ4ÍiÌIjÁ^!xU·dt´Ù]¦K&¥?Aɦøñ”°:@Ù¤H¼BÉ£·:nSI|®lkÔ£SÏáèÀîKù·f=QþXôÊ¿æ5üA93gð©h¬xÐP²&[
çe®!ú8ÙOvÞ=(;,¾m”^uyPjtc47^Q
W6§uÛ
xîA¡·S>Ë¡îgq2CÜY§*KûªZ{o)n0wÍ´ ÿá[,
ÏÙñÕNKx+±Ô±zZpYâÊÀo5_1Sn¼;¢ÝßÃU£:U~q´¨²m½ÄA¾õ]0:Ó Ìç
æñzbkð&GÖ
ª[wi5¬0Æwå©Ú+aªþÁ·-ÝÚc(®Ð»ktÖC?¶é×eë
ËÂ%âÖMºA>º²áª´_t³òmÕ)̺*¤¯¢wlóÊínÜb⤴vAï7ðn«â
¦
9?ÅðÊý©td+ß°¯ÝõÛTf89.¸x@¯jü#u¯J¨a¼ZQõ/³Ó9|¿Äþ6Ò0ÂP8ià0¦£0Ã`¸Uv§ÝòYÚü’è1YÙFª+ê EdY¢úäîa¾eË¥,k&[Ö(YÖ(YÖ L¶¬Q²,©Í˼nã-külYï&ÕX$ÔȲ$Eô7dR]ó®{×a>&ñÉÚ6öIáNÿ¥G
endstream
endobj
24 0 obj
>
>>
/MediaBox [0 0 595 842]
/Contents 25 0 R
>>
endobj
25 0 obj
>
stream
x^½]K«%¹Þß_q×:zg¹P·ºÊ`
íY³*ÜÓsÜÿýâ!EHyʬ6¦]¥:©/CñRDèÿ|ùçy-ÿûí_üº¶øêìvYü«séÿûûË//ÉϾÿüòßü«±¯?ÿò²¼ÿå¹Û¶Ð2¯~]/&wôéòc/ÿýÇe±þí^þóË×ÙâeY;Å)F¹Yááe¹øõÕËÁsÿ´mvoÃÅ|y6^}]/ëZø¯?¼üßSD1¹lL±_QÞY~è/^p{ÔÑ¢¼Â%®¯6]2¬YÅãVP³æIUèqA8!óñ5GÞQû·wÜs²åa»¹ò0¾Òº¢”S:6£¯¯´aZG×t±Ê-Âù¸¬!¾Z_$gãÅOѼ¿õȲ^Ýï³tàÆhp|¶üÿ÷ÜüÇK¦Ëõ/Býë^¼’1¸ÂÎàÁ>¨}}ùÛóPÔÕe
ËüÉPËZþBmªã)ìÌ¿.¶¨ç7£)ãºæ&º°¾_uïë˯ùí C·¸”¤·F×Äï×îy@ ‘”¸ Péçøûµ{¾ üÒizE]Æ>ú,ûTÛÞs¸Ä¬ùß_¸ÉËPÏ2Ejågcä¡_h&÷¤VÅ¥6½{2EÞïe@Ð2ó!ÁóJ”òÜÞ
} )’¡Ô| ñvîÛ~+$:¥#·-þ^ìɹ2Èðü´çvetB¾[/hÞàÎ*@ýVþùÚÆZc/â&ÛqÎ^P¼cøýKysKi8òä S¥½¢”ç1KfLg-*hS_Ò{8g-Píæh
ÕW#aÀÄ
EbÀËåAEOíò2#®zÐÀ|]¿-pÁ{,
·¬ãHC29¥»1EyK¦ù°°ö©Kl|ÀÚB¯Zù°° 3”¼)0×À}WJ»s§ÚkC_[óWgD´ò|ä©th¥½ßã±±dåÅó²`Ðlöß° näßËÏM%a6½cüøF¯Ø=D}7ΪëTm/7p¢Ì>ðêdÉ ¥ì-
~/íM:Ì9^£ ðnñµbÑx ä&Úß^ßÔ)
Источник
11. МКТ и Термодинамика (объяснение явлений)
1. Вспоминай формулы по каждой теме
2. Решай новые задачи каждый день
3. Вдумчиво разбирай решения
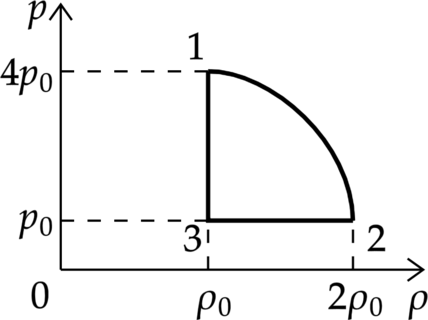
На рисунке показана зависимость давления газа (p) от его плотности (rho) в циклическом процессе, совершаемом 2 моль идеального газа в идеальном тепловом двигателе. Цикл состоит из двух отрезков прямых и четверти окружности.

На основании анализа этого циклического процесса выберите два верных утверждения.
1) В процессе 1−2 температура газа уменьшается.
2) В состоянии 3 температура газа максимальна.
3) В процессе 2−3 объём газа уменьшается.
4) Отношение максимальной температуры к минимальной температуре в цикле равно 8.
5) Работа газа в процессе 3−1 положительна.
“Демоверсия 2017”
1) По уравнению Клапейрона – Менделеева: [p=dfrac{rho}{mu}RT,] где (T) – температура, (mu) – молярная масса газа.
Давление уменьшилось в 4 раза, а плотность увеличилась в 2 раза, следовательно, температура уменьшилась в 8 раз.
Утверждение 1 – (color{green}{small text{Верно}})
2) Аналогично предыдущему пункту [p=dfrac{rho}{mu}RT] Максимальная температура будет в состоянии 1 (давление максимально, плотность минимальна)
Утверждение 2 – (color{red}{small text{Неверно}})
3) В процессе 2 – 3 плотность меньшается, а по формуле: [rho =dfrac{m}{V}] Объем увеличивается
Утверждение 3 – (color{red}{small text{Неверно}})
4) Аналогично пункту 2, минимальность температуры будет достигнута в точке с наименьшим давлением и наибольшей плотностью (т. 2), а отношение температур действительно равно 8
Утверждение 4 – (color{green}{small text{Верно}})
5) В процессе 2 – 3 плотность постоянна, следовательно, объем постоянен и газ не совершает работу.
Утверждение 5 – (color{red}{small text{Неверно}})
Ответ: 14
Сосуд разделён на две равные по объёму части пористой неподвижной перегородкой. В начальный момент времени в левой части сосуда содержится 4 моль гелия, в правой – 40 г аргона. Перегородка может пропускать молекулы гелия и является непроницаемой для молекул аргона. Температура газов одинаковая и остаётся постоянной. Выберите два верных утверждения, описывающих состояние газов после установления равновесия в системе.
1) Концентрация гелия в правой части сосуда в 2 раза меньше, чем аргона.
2) Отношение давления газов в правой части сосуда к давлению газа в левой части равно 1,5.
3) В правой части сосуда общее число молекул газов меньше, чем в левой части.
4) Внутренняя энергия гелия и аргона одинакова.
5) В результате установления равновесия давление в правой части сосуда увеличилось в 3 раза.
“Демоверсия 2020”
Перегородка проницаема только для молекул гелия, поэтому в результате установления равновесия парциальное давление гелия в левой части будет равно парциальному давлению гелия в правой части. Давление газа можно вычислить по формуле: [p=dfrac{nu R T}{V}] Парциальные давления гелия в левой и правой части одинаковы, одинаковы температуры и объёмы частей, следовательно, одинаковы и количества вещества гелия в левой и правой частях сосуда, то есть в левой и правой части сосуда будет содержаться по 2 моля гелия.
Найдём связь концентрации и количества вещества: [n=dfrac{N}{V}=dfrac{nu N_A}{V}] То есть концентрации и количества вещества зависят прямо пропорционально друг от друга, также заметим, что чем больше количество вещества, тем больше и количество молекул.
Найдём количество вещества аргона: [nu_{Ar}=dfrac{m_{Ar}}{mu_{Ar}}=dfrac{40text{ г}}{40text{ г/моль}}=1text{ моль}]
Используя полученное выше, рассмотрим данные в задании утверждения.
Концентрация гелия в два раза больше концентрации аргона в правой части сосуда
1) (color{red}{small text{Неверно}})
Концентрация гелия в два раза больше концентрации аргона в правой части сосуда
2) (color{green}{small text{Верно}})
Отношение давлений: [dfrac{p_text{ п}}{p_text{ л}}=dfrac{nu_text{ г.п}+nu_{Ar}}{nu_text{ г.л}}=dfrac{2text{ моль}+1text{ моль}}{2text{ моль}}=1,5] Где (nu_{text{ г.п.}},nu_{text{ г.л.}}) – количество вещества гелия в правой части, количество вещества гелия в левой части соответственно.
3) (color{red}{small text{Неверно}})
Количество вещества газов в правой части сосуда больше количества вещества газа в левой части сосуда, следовательно, в правой части сосуда общее число молекул газа больше, чем в левой части сосуда.
4) (color{red}{small text{Неверно}})
Внутренняя энергия одноатомного идеального газа может быть вычислена по формуле: [U=dfrac{3}{2}nu R T] Температура газов одинакова. Количество вещества гелия больше количества вещества аргона, следовательно, внутренняя энергия гелия больше внутренней энергии аргона.
5) (color{green}{small text{Верно}})
айдём отношение конечного давления в правой части сосуда к начальному давлению в правой части сосуда: [dfrac{p_{k}}{p_text{ н}}=dfrac{nu_{text{ г.п.}}+nu_{Ar}}{nu_{Ar}}=dfrac{2text{ моль}+1text{ моль}}{1text{ моль}}=3]
Ответ: 25
В цилиндрическом сосуде под поршнем находится газ. Поршень может перемещаться в сосуде без трения. На дне сосуда лежит стальной шарик (см. рисунок). Газ нагревают.
Выберите из предложенного перечня два верных утверждения, верно описывающие данный процесс, и укажите их номера.
1) Объём газа в этом процессе остаётся неизменным.
2) Давление газа в сосуде остаётся неизменным.
3) Плотность газа в этом процессе увеличивается.
4) Сила Архимеда, действующая на шарик, уменьшается.
5) Концентрация молекул газа в сосуде увеличивается.
1) Так как поршень подвижный (не закреплен), то процесс будет происходить при постоянном давлениии.
Уравнение состояния газа: [pV=nu RT] где (nu) — количество вещества, (T) — температура в Кельвинах, (p) — давление газа, (V) — объем, занимаемый газом, (R) — универсальная газовая постоянная. Выразим объем [V=dfrac{nu RT}{p}] При нагревании газа объем увеличивается.
Утверждение 1 — (color{red}{smalltext{Неверно }})
2) Утверждение 2 — (color{green}{smalltext{Верно }})
3) Плотность газа: [rho=dfrac{m}{V}] При нагревании объем увеличивается, значит плотность уменьшается.
Утверждение 3 — (color{red}{smalltext{Неверно }})
4) Сила Архимеда: [F_{text{Арх}}=rho gV] где (rho) — плотность газа, (V) — объем шарика, (g) — ускорение свободного падения. Плотность уменьшается, значит, сила Архимеда уменьшается.
Утверждение 4 — (color{green}{smalltext{Верно }})
5) Концентрация: [n=dfrac{N}{V}] При нагревании газа объем увеличивается, концентрация уменьшается.
Утверждение 5 — (color{red}{smalltext{Неверно }})
Ответ: 24
На (pV)—диаграмме отображена последовательность трёх процессов (1 — 2 — 3) изменения состояния 2 моль идеального газа. 
Из предложенного перечня утверждений выберите два правильных и укажите их номера.
1) В процессе 1 газ отдаёт положительное количество теплоты.
2) Процесс 2 является изотермическим.
3) В процессе 3 газ совершает работу.
4) В процессе 2 происходит расширение газа при постоянной температуре.
5) В процессе 1 происходит сжатие газа при постоянной температуре.
Работа газа находится как площадь под графиком 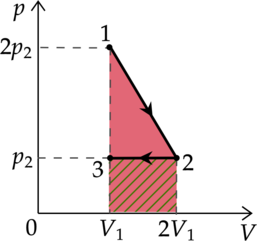
1) Первое начало термодинамики: [Q=Delta U+A] где (Delta U) — изменение внутренней энергии, (A) — работа газа, (Q) — количество теплоты, полученное газом. (Delta U=0), так как температура в процессе 1 не изменяется. При увеличении давления в изотермическом процессе объём уменьшается. (Delta V<0), следоватлеьно, (A<0). Таким образом, (Q<0), то есть газ отдает кол-во теплоты в данном процессе.
Утверждение 1 — (color{green}{smalltext{Верно }})
2) В процессе 2 температура увеличивается.
Утверждение 2 — (color{red}{smalltext{Неверно }})
3) (p=const), следовательно (Vsim T)
Температура уменьшается, то есть объем тоже уменьшается, (Delta V<0), (A<0)
Утверждение 3 — (color{red}{smalltext{Неверно }})
4) В процессе 2 температура увеличивается.
Утверждение 4 — (color{red}{smalltext{Неверно }})
5) Температура в процессе 1 не изменяется. По закону Бойля-Мариотта (p V=const) так как давление увеличивается объём уменьшается.
Утверждение 5 —(color{green}{smalltext{Верно }})
Ответ: 15
На рисунке показан график циклического процесса, проведённого с одноатомным идеальным газом, в координатах (V-T), где (V) — объём газа, (T) — абсолютная температура газа. Количество вещества газа постоянно. 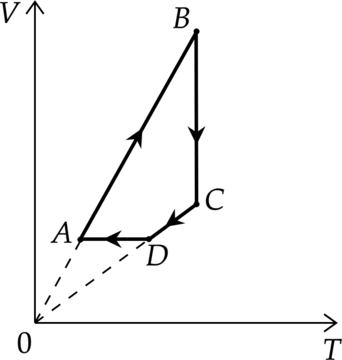
Из приведённого ниже списка выберите два правильных утверждения, характеризующие процессы на графике, и укажите их номера.
1) В состоянии (B) концентрация газа максимальна.
2) В процессе (AB) газ отдаёт некоторое количество теплоты.
3) В процессе (BC) внутренняя энергия газа увеличивается.
4) Давление газа в процессе (CD) постоянно, при этом внешние силы совершают над газом положительную работу.
5) В процессе (DA) давление газа изохорно уменьшается.
1) В точке (B) объем максимален, а концентрация минимальна:
Утверждение 1 —(color{red}{smalltext{Неверно }})
2) Первое начало термодинамики: [Q=Delta U+A] где (Delta U) — изменение внутренней энергии, (A) — работа газа, (Q) — количество теплоты, полученное газом. В процессе (AB) работа равна (0), температура увеличивается, то есть (Delta U>0), значит (Q>0), то есть газ получает тепло
Утверждение 2 — (color{red}{smalltext{Неверно }})
3) Процесс (BC) — изотермический. Внутренняя энергия не меняется.
Утверждение 3 — (color{red}{smalltext{Неверно }})
4) Процесс (СD) — изобарное сжатие. При уменьшении объема внешние силы совершают положительную работу.
Утверждение 4 — (color{green}{smalltext{Верно }})
5) Процесс (DA) — изохорное охлаждение ((psim T)). Следовательно, при уменьшении температуры давление уменьшается.
Утверждение 5 — (color{green}{smalltext{Верно }})
Ответ: 45
Идеальный газ перевели из состояния 1 в состояние 3 так, как показано на графике зависимости давления р газа от объёма V. Количество вещества газа при этом не менялось. 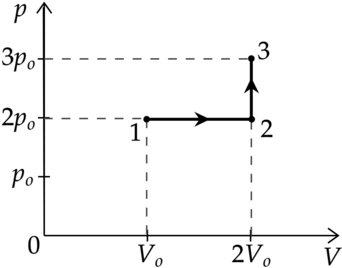
Из приведённого ниже списка выберите два правильных утверждения, характеризующие процессы на графике.
1)Абсолютная температура газа минимальна в состоянии 2.
2)В процессе 1-2 абсолютная температура газа уменьшилась в 2 раза.
3)В процессе 2-3 абсолютная температура газа уменьшилась в 1,5 раза.
4)Плотность газа максимальна в состоянии 1.
5)В ходе процесса 1-2-3 средняя квадратичная скорость теплового движения молекул газа увеличилась в (sqrt{3}) раза.
1) Уравнение состояния газа: [pV=nu RT] где (p) — давление газа, (V) — объем, занимаемый газом, (nu) — количество вещеста, (R) — универасальная газовая постоянная, (T) — температура. Температура максимальна там, где максимально произведение (pV), поэтому из графика видно, что (T_1 – min), (T_3 – max), (T_1<T_2<T_3)
Утверждение 1 — (color{red}{smalltext{Неверно }})
2) Процесс 1-2 — изобарное расширение ((Vsim T)). Объем увеличился в 2 раза, то есть температура тоже увеличилась в 2 раза.
Утверждение 2 — (color{red}{smalltext{Неверно }})
3) Процесс 2-3 — изохорное нагревание. (V=const), следовательно (psim T) Давление увеличивается в 1,5 раза, то есть температура тоже увеличивается в 1,5 раза.
Утверждение 3 — (color{red}{smalltext{Неверно }})
4) В точке 1 — объем минимален, следовательно, плотность там максимальна.
Утверждение 4 — (color{green}{smalltext{Верно }})
5) [E_{k}=dfrac{3}{2}kT] [dfrac{m_0 v^2}{2}=dfrac{3}{2}kT] где (m_0) — масса газа, (v^2) средняя квадратичная скорость [v^2sim T] [vsim sqrt{T}] Температура в процессе 1-2-3 увеличилась в 3 раза, значит средняя квадратичная скорость увеличилась в (sqrt{3}) раз
Утверждение 5 — (color{green}{smalltext{Верно }})
Ответ: 45
Сосуд разделён на две равные по объёму части пористой неподвижной перегородкой. В левой части сосуда содержится 40 г неона, в правой — 2 моль гелия. Перегородка может пропускать молекулы гелия и является непроницаемой для молекул неона. Температура газов одинакова и остаётся постоянной.
Выберите два верных утверждения, описывающих состояние газов после установления равновесия в системе.
1) Внутренняя энергия гелия в сосуде меньше, чем внутренняя энергия неона.
2) Концентрация гелия в левой части сосуда в 2 раза больше концентрации неона.
3) В левой части сосуда общее число молекул газов в 3 раза больше, чем в правой части.
4) Внутренняя энергия гелия в сосуде в конечном состоянии меньше, чем в начальном.
5) В конечном состоянии давление в левой части сосуда в 3 раза больше, чем в правой.
1) Молярная масса неона (M=20) г/моль. Количество неона: [nu=dfrac{m}{M}=dfrac{40text{ г}}{20text{ г/моль}}=2 text{ моль}] Гелий займет все пространство сосуда, значит в левой части будет 3 моля вещества (1 моль гелия и 2 моль неона).
В правой части будет тоже 1 моль гелия.
Внутренняя энергия газа: [U=dfrac{i}{2}nu RT] Газы находятся при одинаковой температуре, количество гелия равно количеству неона. Внутренняя энергия гелия равна внутренней энергии неона
Утверждение 1 — (color{red}{smalltext{Неверно }})
2) В левой части сосуда количество гелия в два раза меньше количества неона. Следовательно, концентрация гелия в два раза меньше концентрации неона.
Утверждение 2 — (color{red}{smalltext{Неверно }})
3) Так как количество вещества в левой части сосуда больше в 3 раза, чем в правой, то и количество молекул также больше в 3 раза.
Утверждение 3 — (color{green}{smalltext{Верно }})
4) Так как температура гелия и общее количество гелия в сосуде не изменилось, то и внутреннняяя энергия не поменялась.
Утверждение 4 — (color{red}{smalltext{Неверно }})
5) Давление газа: [p=nkT] Так как кол-во вещества в левой части сосуда больше в 3 раза, чем в правой, температуры одинаковые, то давление в конечном состоянии больше в левой части в 3 раза, чем в правой.
Утверждение 5 — (color{green}{smalltext{Верно }})
Ответ: 35
Источник
