В сосуде разделенном на равные части неподвижной непроницаемой
Теплоизолированный сосуд разделен перегородкой на две равные части. В одной половине находится идеальный газ, в другой – вакуум. Перегородку мгновенно убирают, и газ заполняет весь объем. В этом необратимом процессе энтропия газа…
Предмет: Физика (22207 вопросов)
Помог сайт? Помоги другу:
- уменьшается
- может увеличиваться и уменьшаться
- не изменяется
- увеличивается
Тип вопроса: Вопрос с одним правильными вариантом
Вопрос задал(а): Анонимный пользователь, 12 Ноябрь 2020 в 20:37
На вопрос ответил(а): Анастасия Степанова, 12 Ноябрь 2020 в 20:37
Похожие вопросы
Теплоизолированный сосуд разделен перегородкой на две равные части. В одной половине находится идеальный газ, в другой – вакуум. Перегородку мгновенно убирают, и газ заполняет весь объем. В этом необратимом процессе энтропия газа…
не изменяется
может увеличиваться и уменьшаться
уменьшается
увеличивается
Теплоизолированный сосуд разделен перегородкой на две равные части. В одной половине находится идеальный газ, в другой – вакуум. Перегородку мгновенно убирают, и газ заполняет весь объем. В этом необратимом процессе энтропия газа…
может увеличиваться и уменьшаться
уменьшается
не изменяется
увеличивается
Теплоизолированный сосуд разделен перегородкой на две равные части. В одной половине находится идеальный газ, в другой – вакуум. Перегородку мгновенно убирают, и газ заполняет весь объем. В этом необратимом процессе энтропия газа…
может увеличиваться и уменьшаться
не изменяется
уменьшается
увеличивается
В сосуде, разделенном на равные части неподвижной непроницаемой перегородкой находится газ. Температуры газа в каждой части сосуда равны, по массе газа в левой части больше, чем в правой М1>М2.
Функция распределения скоростей молекул газа в сосуде будет описываться кривыми…
Источник
Число молекул, относительные скорости которых заключены в данном интервале (распределение Максвелла)
(II.10)
Относительная скорость молекул
(II.11)
Формула изменения концентрации молекул с высотой
(II.12)
Барометрическая формула
(II.13)
где и – давление, и – концентрация газа на высоте и ;
– молярная масса газа; – ускорение свободного падения.
Средняя квадратичная скорость молекул
.(II.14)
Средняя арифметическая скорость молекул
.(II.15)
Наиболее вероятная скорость
,(II.16)
где – масса одной молекулы.
ЗАДАЧА № II.33В законе распределения Максвелла для газовых молекул по скоростям кривая распределения асимптотически приближается к оси скоростей. Означает ли это, что молекулы газа, пусть с малой вероятностью, но могут иметь сколь угодно большие скорости?
Ответ: Скорость молекул ограничена определенным значением энергии теплового движения газа при данной температуре.
ЗАДАЧА № II.34 Возможны ли в газе с температурой К неподвижные молекулы?
Ответ: Их вероятность исчезающее мала, т.к. кривая распределения Максвелла проходит через начало координат.
ЗАДАЧА № II. 35Какой вид приобретет барометрическая формула на большой высоте?
Ответ:С высотой ускорение свободного падения уменьшается, поэтому необходимо использовать потенциальную энергию гравитационного поля
, и барометрическая формула примет вид , где – масса Земли, – масса молекулы газа.
ЗАДАЧА № II.36Как можно трактовать нормировку функции распределения Максвелла, а именно
Ответ:Как достоверное событие, имеющее вероятность равную единице.
ЗАДАЧА №II.37Почему отличаются по своему значению средняя квадратичная, средняя арифметическая и наиболее вероятная скорости газовых молекул?
Ответ:Это вызвано асимметричностью кривой распределения Максвелла.
ЗАДАЧА№ II.38Почему с повышением температуры газа вместе с расширением кривой распределения понижается ее максимум?
Ответ: Это следует из условия нормировки, а следовательно из постоянства площади под кривой.
ЗАДАЧА № II.39Влияют ли на максвелловское распределение молекул по скоростям параметры состояния газа?
Ответ:Влияет только температура.
ЗАДАЧА № II.40Если число молекул в сосуде увеличили, не изменив температуры, то как изменится число молекул, обладающих наиболее вероятной скоростью в максвелловском распределении молекул по скоростям?
Ответ: Число молекул, обладающих наиболее вероятными скоростями, увеличится.
ЗАДАЧА № II.41 В трех одинаковых сосудах при равных условиях находится одинаковое количество азота (N2), гелия (He), и водорода (H2). На рис. 27 дано распределение скоростей этих молекул. Каким кривым распределения соответствуют молекулы водорода и азота?
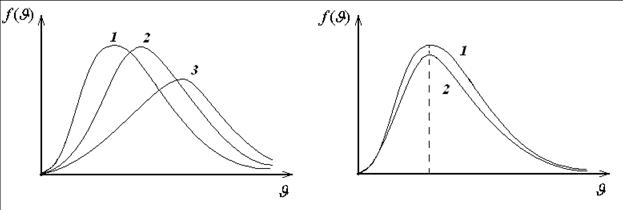
Рисунок 27- Распределение скоростей Рисунок 28- Кривые 1 и 2
молекул
Ответ: Водороду – 3, азоту – 1. Наиболее вероятная скорость , она зависит от молярной массы газа и будет наименьшей для азота, ( г/моль) и наибольшей у водорода ( г/моль).
ЗАДАЧА № II.42 В сосуде, разделенном на равные части неподвижной непроницаемой перегородкой, находится газ. Температуры газа в каждой части сосуда равны, масса газа в левой части больше, чем в правой . Какими кривыми (рис.28) будут описываться функции распределения молекул по скоростям для молекул газа в правой и левой частях сосуда?
Ответ: Газ в обеих частях сосуда одинаковый, температуры равны, следовательно наиболее вероятные скорости молекул тоже равны . Массы разные . В большей массе будет большее число молекул, следовательно, будет больше площадь под кривой функции распределения
. Кривая 1 – для левой части, кривая 2 – для правой части.
ЗАДАЧА № II.43 Определить долю молекул водорода, модули скоростей которых при температуре 27° С лежат в интервале от 1898 м/с до 1902 м/с.
Дано: кг/моль;
К;
м/с;
м/с.
Найти:
Решение
В данной задаче удобнее воспользоваться распределением молекул по относительным скоростям. Доля молекул , относительные скорости которых заключены в интервале от до , определяется формулой
, (1)
где – наиболее вероятная скорость; .
С учетом этих выражений формула (1) примет вид
.
Для удобства сначала вычислим
(м/с),
и отношение скоростей .
Подставим численные значения в (1) и найдем долю молекул водорода, модули скоростей которых лежат в интервале от до
.
ЗАДАЧА № II.44Броуновские частицы с массой 4 фгведут себя в тепловом движении подобно гигантским молекулам, и к ним можно применить закономерности молекулярно-кинетической теории. Исходя из этого, определить, во сколько раз уменьшится концентрация броуновских частиц при увеличении высоты на 1 мм. Температуру принять равной 300 К.
Дано: фг г кг;
мм м;
К.
Найти:
Решение
Для броуновских частиц воспользуемся распределением молекул по
высоте (распределение Больцмана)
,
где и – концентрация молекул на высоте и на высоте , соответственно. Выразим
Прологарифмируем и подставим численные значения,
.
Итак, то есть концентрация частиц уменьшится в раз.
ЗАДАЧА № II.45 На какой высоте над уровнем моря атмосферное давление составляет 78 кПа, если температура воздуха 170С и не меняется с высотой, а давление на уровне моря нормальное? Найти число частиц в единице объема на этой высоте.
Дано: C К;
Па;
Па;
кг/моль.
Найти:
Решение
Если температура не меняется с высотой, то для нахождения давления можно воспользоваться барометрической формулой (II.13)
логарифмируя эту формулу, получаем
Отсюда находим
м; м-3.
ЗАДАЧА № II.46Найти число молекул водорода, заключенных в 1см3 при нормальных условиях, а также число молекул значения скоростей которых лежат в интервале между 399 и 401 м/с.
Дано: см3 м3;
Па;
К;
м/с;
м/с;
кг/моль;
Найти:
Решение
Число молекул можно найти из распределения Максвелла, заданного в виде уравнения (II.10)
Для всех газов при нормальных условиях число молекул в 1 см3 одно и то же и равно см-3 (число Лошмидта).
Вычислим значения величин, входящих в распределение Максвелла
, м/с;
м/с; м/с;
ЗАДАЧА № II.47Температура окиси азота (NO) 300 К. Определить долю молекул, скорость которых лежит в интервале от 820 м/с до 830 м/с.
Дано: К;
м/с;
м/с;
кг/моль.
Найти:
Решение
Рассматриваемый газ находится в равновесном состоянии. Согласно распределению Максвелла, относительное число молекул, скорость которых заключена в интервале от до , ,
где – функция распределения Максвелла, которую можно представить в виде: где м/с.
Тогда
с/м.
Аналогично подсчитаем с/м.
В условии задачи требуется определить долю молекул, скорости которых лежат в диапазоне м/с.
Если в этом пределе функцию Максвелла можно с достаточной степенью точности считать постоянной, то искомая величина может быть рассчитана по приближённой формуле
т.е. Это значит, что при использовании этой формулы допускается ошибка, относительная величина которой
.
Следовательно, с указанной степенью точности можно использовать равенство , или .
Источник
Разбор 11 задания ЕГЭ 2020 по физике из демонстрационного варианта. Проверяемые элементы содержания: МКТ, термодинамика (объяснение явлений; интерпретация результатов опытов, представленных в виде таблицы или графиков).
Сосуд разделен на две равные по объему части пористой неподвижной перегородкой. В начальный момент времени в левой части сосуда содержится 4 моль гелия, в правой — 40 г аргона. Перегородка может пропускать молекулы гелия и является непроницаемой для молекул аргона. Температура газов одинаковая и остается постоянной. Выберите два верных утверждения, описывающих состояние газов после установления равновесия в системе.
1) Концентрация гелия в правой части сосуда в 2 раза меньше, чем аргона.
2) Отношение давления газов в правой части сосуда к давлению газа в левой части равно 1,5.
3) В правой части сосуда общее число молекул газов меньше, чем в левой части.
4) Внутренняя энергия гелия и аргона одинакова.
5) В результате установления равновесия давление в правой части сосуда увеличилось в 3 раза.
Перегородка проницаема только для молекул гелия, поэтому в результате установления равновесия парциальное давление гелия в левой части будет равно парциальному давлению гелия в правой части. Давление газа можно вычислить по формуле: p = νRT/V Парциальные давления гелия в левой и правой части одинаковы, одинаковы температуры и объемы частей, следовательно, одинаковы и количества вещества гелия в левой и правой частях сосуда, то есть в левой и правой части сосуда будет содержаться по 2 моля гелия.
Найдем связь концентрации и количества вещества: n = N/V = νNA/V. То есть концентрации и количества вещества зависят прямо пропорционально друг от друга, также заметим, что чем больше количество вещества, тем больше и количество молекул.
Найдем количество вещества аргона: νAr = mAr/μAr = 40 г/40 г/моль = 1 моль.
Теперь, с помощью полученных результатов, найдем верные утверждения.
1) Концентрация гелия в правой части сосуда в 2 раза меньше, чем аргона. Неверно!
Концентрация гелия в два раза больше концентрации аргона в правой части сосуда. Утверждение неверно.
2) Отношение давления газов в правой части сосуда к давлению газа в левой части равно 1,5. Верно!
Найдем отношение давлений газов в правой и левой частях сосуда:
pп/pл = νг.п. + νAr/νг.л. = 2 моль + 1 моль/2 моль = 1,5
Здесь νг.п., νг.л., νAr — количество вещества гелия в правой части, количество вещества гелия в левой части, количество вещества аргона, соответственно. Утверждение верно.
3) В правой части сосуда общее число молекул газов меньше, чем в левой части. Неверно!
Количество вещества газов в правой части сосуда больше количества вещества газа в левой части сосуда, следовательно, в правой части сосуда общее число молекул газа больше, чем в левой части сосуда. Утверждение неверно.
4) Внутренняя энергия гелия и аргона одинакова. Неверно!
Внутренняя энергия одноатомного идеального газа может быть вычислена по формуле: U = 3/2νRT. Температура газов одинакова. Количество вещества гелия больше количества вещества аргона, следовательно, внутренняя энергия гелия больше внутренней энергии аргона. Утверждение неверно.
5) В результате установления равновесия давление в правой части сосуда увеличилось в 3 раза. Верно!
Найдем отношение начального давления в правой части сосуда к конечному давлению в правой части сосуда:
pк/pн = νг.п. + νAr/νAr = 2 моль + 1 моль/1 моль = 3. Утверждение 5 верно.
Ответ:
25
Источник

Молекулярная физика
| В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота A) Распределение скоростей молекул водорода будет описывать кривая | A)
| ||||
| В трех одинаковых сосудах находится одинаковое количество газа, причем T1 >T2>T3 A) Распределение скоростей молекул в сосуде с температурой T1описывает кривая B) Распределение скоростей молекул в сосуде с температурой T2описывает кривая C) Распределение скоростей молекул в сосуде с температурой T3описывает кривая | A)
| ||||
| В сосуде, разделенном на равные части неподвижной непроницаемой перегородкой, находится газ. Температуры газа в каждой части сосуда равны, по массе газа в левой части больше, чем в правой M1 > M2. Функция распределения скоростей молекул газа в сосуде будет описываться кривыми | |||||
| На рисунке представлен график функции (распределения Максвелла), где f (υ) = dN/(Ndυ) – доля молекул, скорости которых заключены в интервале скоростей от υ до υ+dυ в расчете на единицу этого интервала. Для этой функции верным утверждением является… | 1. С ростом температуры площадь под кривой растет. 2. С ростом температуры максимум кривой смещается вправо. 3. С ростом температуры величина максимума растет. A) при понижении температуры величина максимума уменьшается B) положение максимума кривой зависит как от температуры, так и от природы газа C) при понижении температуры площадь под кривой уменьшается | ||||
| На рисунке представлен график функции (распределения Максвелла). Используя максвелловскую функцию распределения молекул по скоростям, можно: | 1. Доказать, что молекулы движутся с определенной скоростью u. 2. Сделать вывод о направлении скорости u. 3. Рассчитать вероятность того, что скорость молекул находится в интервале от u до u+du 4. Рассчитать вероятность того, что скорость молекул равна u. 5. Доказать, что скорости молекул отличны друг от друга, но постоянны. | ||||
| На рисунке представлен график функции (распределения Максвелла), где f (υ) = dN/(Ndυ) – доля молекул, скорости которых заключены в интервале скоростей от υ до υ+dυ в расчете на единицу этого интервала. Если, не меняя температуры взять другой газ с меньшей молярной массой и таким же числом молекул, то… | A) максимум кривой сместится вправо в сторону больших скоростей B) площадь под кривой уменьшится C) величина максимума увеличится | ||||
| На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где – доля молекул, скорости которых заключены в интервале скоростей от до в расчете на единицу этого интервала. Для этой функции верными являются утверждения, что … |
| ||||
| На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где – доля молекул, скорости которых заключены в интервале скоростей от до в расчете на единицу этого интервала. Для этой функции неверными являются утверждения, что … |
| ||||
| На рисунке представлены графики зависимости концентрации молекул идеального газа от высоты над уровнем моря для двух разных температур – (распределение Больцмана). Для графиков этих функций верными являются утверждения, что … | |||||
| Зависимости давления идеального газа во внешнем однородном поле силы тяжести от высоты для двух разных температур представлены на рисунке. Для графиков этих функций неверными являются утверждения, что … | |||||
| На рисунке представлены графики функции распределения молекул идеального газа по скоростям (распределение Максвелла), где – доля молекул, скорости которых заключены в интервале скоростей от до в расчете на единицу этого интервала. Для этих функций верными являются утверждения, что … |
| ||||
Средняя энергия молекул
| Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. A) Средняя кинетическая энергия молекул гелия (Не) равна… B) При условии, что имеют место только поступательное и вращательное движение, средняя энергия молекул азота (N2) равна … | 1/2kT 3/2kT 5/2kT 6/2kT 7/2kT | ||||
| Средняя кинетическая энергия молекулы идеального газа при температуре Т равна ε = i/2kТ. Здесь i=nn+nвр+2nk, где nn,nвр и 2nk – степени свободы поступательного, вращательного и колебательного движений молекулы. A) При условии, что имеет место только поступательное и вращательное движение, для молекулярного водорода средняя кинетическая энергия молекул равна… B) При условии, что имеют место только поступательное и вращательное движение, для водяного пара (Н2О) число i равно … C) При условии, что имеют место только поступательное и вращательное движение, для водорода (Н2) число i равно … D) При условии, что имеют место только поступательное и вращательное движение, средняя энергия молекул азота (N2) равна … | A) 1/2kT 3/2kT 5/2kT 6/2kT B) C) D) | ||||
| Выберите верное утверждение: В смеси газов, содержащей молекулы разного сорта, будут одинаковыми… | A) средняя скорость молекул; B) импульс молекул; C) температура; D) давление | ||||
| При комнатной температуре отношение молярных теплоемкостей при постоянном давлении и постоянном объеме равно для … |
| ||||
| В соответствии с законом равномерного распределения энергии по степеням свободы средняя кинетическая энергия молекулы идеального газа при температуре T равна: . Здесь , где , и – число степеней свободы поступательного, вращательного и колебательного движений молекулы соответственно. Для гелия ( ) число i равно … | |||||
| Кинетическая энергия (в Дж) всех молекул в 2 г неона при температуре 300 К равна … | |||||
| Средняя кинетическая энергия молекул газа при температуре зависит от их конфигурации и структуры, что связано с возможностью различных видов движения атомов в молекуле и самой молекулы. При условии, что имеет место поступательное, вращательное движение молекулы как целого и колебательное движение атомов в молекуле, средняя кинетическая энергия молекулы кислорода ( ) равна … | |||||
Законы термодинамики
| На рисунке изображен цикл Карно в координатах (T,S), где S-энтропия. A) Изотермическое расширение происходит на этапе… | 1-2 2-3 3-4 4-1 | ||||
| Процесс, изображенный на рисунке, в координатах (T,S), где S- энтропия, является… |
| ||||
| На (P,V) – диаграмме изображен циклический процесс. A) На участках BC-CD температура… | A) 1. повышается 2. понижается 3. на BC – понижается, на CD – повышается 4. на BC – повышается, на CD – понижается B) 1. повышается 2. на DA – понижается, на AB – повышается 3. на DA – повышается, на AB – понижается 4. понижается | ||||
| Тепловые машины работают по циклам, представленным на рисунках. Какая из них имеет максимальный КПД при одинаковых температурах нагревателей и холодильников? ( р – давление; V– объем; на рис. Г изображен цикл Карно). | 1. A; 2. Б; 3. В; 4. Г; 5. Все имеют одинаковый КПД. | ||||
| Энтропия неизолированной термодинамической системы при поступлении в неё тепла в ходе обратимого процесса … | только убывает только остается постоянной только увеличивается | ||||
| Двухатомному идеальному газу в результате изобарического процесса подведено количество теплоты . На увеличение внутренней энергии газа расходуется часть теплоты , равная … | 0,75 0,29 0,25 0,71 | ||||
| В процессе обратимого изохорического охлаждения постоянной массы идеального газа его энтропия … | уменьшается увеличивается не меняется | ||||
| Идеальный газ расширяясь, переходит из одного состояния в другое тремя способами: 1. изобарически; 2. изотермически; 3. адиабатически. Совершаемые в этих процессах работы соотносятся между собой следующим образом | A1>A2 >A3 A1=A2 =A3 A1>A2 <A3 A1<A2 >A3 | ||||
| Энтропия неизолированной термодинамической системы в процессе плавления вещества в ней … | увеличивается убывает может как убывать, так и оставаться постоянной остается постоянной | ||||
| При адиабатическом сжатии идеального газа … | температура и энтропия возрастают температура не изменяется, энтропия возрастает температура возрастает, энтропия не изменяется температура возрастает, энтропия убывает | ||||
| Для необратимого процесса в неизолированной термодинамической системе неравенство Клаузиуса имеет вид … | |||||
| Площадь фигуры ABCD численно равна работе, совершаемой идеальным газом при изобарном расширении, на рисунке … | |||||
| При изотермическом расширении давление газа растет, при этом энтропия… | увеличивается равна нулю уменьшается не изменяется | ||||
| КПД цикла Карно равен 60%. Если на 20% уменьшить температуру нагревателя и на 20% увеличить температуру холодильника, КПД (в %) достигнет значения … | |||||
| При плавлении вещества энтропия неизолированной термодинамической системы … |
| ||||
| В ходе необратимого процесса при поступлении в неизолированную термодинамическую систему тепла для приращения энтропии верным будет соотношение … | |||||
| Если количество теплоты, получаемое рабочим телом от нагревателя, увеличится в 2 раза, то коэффициент полезного действия тепловой машины … | |||||
| На рисунке изображен цикл Карно в координатах (T, S), где S – энтропия. Адиабатное сжатие происходит на этапе … | |||||
| При изотермическом расширении 0,5 моля газа при температуре 200 К объем увеличился в раз ( ). Работа газа (в Дж) равна … | |||||
| Диаграмма циклического процесса идеального одноатомного газа представлена на рисунке. Работа газа за цикл (в кДж) равна … | |||||
| Диаграмма циклического процесса идеального одноатомного газа представлена на рисунке. Отношение работы газа за цикл к работе при охлаждении газа по модулю равно … | |||||
| На (P,V)-диаграмме изображены 2 циклических процесса. Отношение работ , совершенных в этих циклах, равно … | |||||
Явления переноса
| Явление диффузии имеет место при наличии градиента… | A) температуры B) потенциала электростатического поля; C) концентрации D) скорости слоев жидкости или газа. |
| Явление диффузии характеризует перенос: | A) электрического заряда; B) массы; C) энергии; D) импульса направленного движения. |
| Явление внутреннего трения имеет место при наличии градиента… | A) температуры; B) потенциала электростатического поля; C) концентрации; D) скорости слоев жидкости или газа. |
| Явление теплопроводности имеет место при наличии градиента… | A) температуры; B) потенциала электростатического поля; C) концентрации; D) скорости слоев жидкости или газа. |
| В жидкости вектор градиента температуры направлен вдоль оси +ОХ. В каком направлении происходит перенос тепла? | + OZ – ОХ – OZ + ОУ + OХ |
| В жидкости вектор градиента скорости слоев направлен вдоль оси +ОZ. В каком направлении происходит перенос импульса молекул? | + OZ – ОХ – OZ + ОУ + OХ |
| На рис. приведена фазовая диаграмма состояния воды. A) Какой процесс содержит переход «жидкость- тв. тело»? B) Какой процесс содержит переходы «жидкость- газ»? | 1) Х-Х 2) М-М 3) Z-Z 4) Y-Y 5) N-N |
| Укажите, какие вещества имеют температуру плавления | 1. полиэтилен; 2. поваренная соль; 3. смола; 4. сливочное масло; 5. стекло. |
| Выберите неверное утверждение: Металл отличается от диэлектрика тем, что … | 1. имеет хорошую теплопроводность; 2. имеет хорошую электропроводность; 3. при Т=0 К электроны в диэлектрике находятся на самом низком энергетическом уровне, а в металле распределены по всем энергетическим уровням согласно статистике Ферми-Дирака; 4. энергетический спектр электронов в металлах не имеет запрещенной зоны; 5. даже при низких Т металл имеет свободные электроны, которые участвуют в проводимости. |
| Выберите верное утверждение. | Электрическое сопротивление металлов при увеличении температуры: А) Увеличивается из-за увеличения скорости хаотического движения электронов. Б) Уменьшается из-за увеличения скорости хаотического движения электронов. В) Увеличивается из-за увеличения амплитуды колебаний положительных ионов кристаллической решетки. Г) Уменьшается из-за увеличения амплитуды колебаний положительных ионов кристаллической решетки. Д) Уменьшается из-за увеличения концентрации свободных носителей электрического заряда. |
Дата добавления: 2015-11-05; просмотров: 2677 | Нарушение авторских прав | Изречения для студентов
Читайте также:
Рекомендуемый контект:
Поиск на сайте:
© 2015-2021 lektsii.org – Контакты – Последнее добавление
Источник
