В сосуде содержится кислород массой 48 г треть молекул которого

Решение задач на количественные характеристики вещества:
количества вещества, массу и объем
Количество вещества (ν) связано с числом структурных единиц (N) в образце вещества, его массой (m) и объемом (V) — для газообразных веществ при н. у. — следующими уравнениями:
 в которых
в которых
Vm = 22,4 л/моль (мл/ммоль, м3/кмоль) при н.у.,
NA = 6,02 • 1023 (постоянная Авогадро),
а молярная масса (М) численно равна относительной молекулярной массе вещества.
Цитаты из пособия «Задачи по химии 8-9 кл.» (авт. О.С. Габриелян и др.) использованы в учебных целях. Ссылка на покупку книги указана в конце конспекта.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
№ 1.
Определите абсолютную массу (в г) одной молекулы воды.
 Ответ: m (молекулы Н2O) = 2,99 • 10–23 г.
Ответ: m (молекулы Н2O) = 2,99 • 10–23 г.
№ 2.
Определите массу порции оксида серы (VI), содержащей 7,224 • 1023 атомов кислорода.

Ответ: m(SO3) = 32 г.
№ 3.
Сколько атомов азота содержится в оксиде азота (I), объем которого (н. у.) равен 20,16 л?
 Ответ. N(N) = 10,836 • 1023.
Ответ. N(N) = 10,836 • 1023.
№ 4.
Определите объем (н. у.) оксида углерода (IV), в котором содержится столько же атомов кислорода, сколько их содержится в 48 г карбоната кальция.

Ответ. V(СO2) = 16,12 л.
№ 5.
Определите относительную плотность сероводорода по водороду и по воздуху.

Ответ: DH2(H2S) = 17; Dвозд(H2S) = 1,17.
№ 6.
Плотность газа по кислороду равна 0,875. Определите число молекул, содержащихся в 15,4 г этого газа.

Ответ. N(газа) = 3,311 • 1023.
ЗАДАЧИ с КРАТКИМ ОТВЕТОМ
№ 7. Сплав содержит 16 г меди и 11,2 г железа. Атомов какого метала будет больше в данном образце сплава?
№ 8. Смешали 16,8 г азота и 15,68 л (н. у.) водорода. Какое суммарное число молекул обоих газов будет содержаться в данной смеси?
№ 9. Чему равна масса порции хлорида бария, содержащая 1,3244 • 1024 ионов хлора?
№ 10. Какую массу должен иметь образец нитрата калия, чтобы в нем было столько же атомов кислорода, сколько их содержится в образце сульфата натрия массой 21,3 г?
№ 11. Сколько атомов хлора содержится в смеси, состоящей из 16,68 г хлорида фосфора (V) и 16,5 г хлорида фосфора (III)?
№ 12. Вычислите массу смеси, содержащей 672 мл (н. у.) оксида азота (I), 0,125 моль оксида азота (II) и 1,15 г оксида азота (IV). Сколько атомов азота будет содержаться в этой смеси?
№ 13. Молекула некоторого газа имеет массу 6,063* 10–23г. Определите плотность данного газа по гелию.
№ 14. Вычислите плотность газа по азоту, если 1 л (н. у.) этого газа имеет массу 1,7857 г.
№ 15. Плотность газа по воздуху равна 2,207. Найдите плотность этого газа по хлору и массу одной молекулы этого газа (в г).
№ 16. Масса порции оксида алюминия равна массе порции оксида кремния (IV). В какой порции будет содержаться больше атомов кислорода?
№ 17. Порции метана СН4 и аммиака NH3 содержат одинаковое число атомов водорода. Какая порция будет иметь большую массу?
№ 18. Десять молекул газа имеют массу 6,063 * 10–22г. Определите плотность данного газа по водороду.
№ 19. Определите массу и объем (н. у.) аммиака, содержащего столько же атомов водорода, сколько их содержится в 2,55 г сероводорода.
Решение задач на основные количественные характеристики вещества. Выберите дальнейшие действия:
- Перейти к следующей теме: Решение задач с долей вещества в смеси, в соединении.
- Вернуться к списку конспектов по Химии.
- Проверить знания по Химии.
- Купить книгу Задачи по химии и способы их решения. 8-9 кл. / О.С. Габриелян и др. — М.: Дрофа.
Источник
Ñîðîêèí Â.Â., Çàãîðñêèé Â.Â., Ñâèòàíüêî
È.Â.Çàäà÷è õèìè÷åñêèõ îëèìïèàä.
1.2. Ãàçîâûå çàêîíû
Çàâèñèìîñòü ìåæäó äàâëåíèåì è îáúåìîì
èäåàëüíîãî ãàçà ïðè ïîñòîÿííîé òåìïåðàòóðå
ïîêàçàíà íà ðèñ. 1.
Äàâëåíèå è îáúåì îáðàçöà ãàçà îáðàòíî
ïðîïîðöèîíàëüíû, ò. å. èõ ïðîèçâåäåíèÿ ÿâëÿþòñÿ
ïîñòîÿííîé âåëè÷èíîé: pV = const. Ýòî ñîîòíîøåíèå
ìîæåò áûòü çàïèñàíî â áîëåå óäîáíîì äëÿ ðåøåíèÿ
çàäà÷ âèäå:
p1V1 = p2V2 (çàêîí
Áîéëÿ-Ìàðèîòòà).
Ïðåäñòàâèì ñåáå, ÷òî 50 ë ãàçà (V1), íàõîäÿùåãîñÿ
ïîä äàâëåíèåì 2 àòì (p1), ñæàëè äî îáúåìà 25 ë (V2),
òîãäà åãî íîâîå äàâëåíèå áóäåò ðàâíî:
Çàâèñèìîñòü ñâîéñòâ èäåàëüíûõ ãàçîâ îò
òåìïåðàòóðû îïðåäåëÿåòñÿ çàêîíîì Ãåé-Ëþññàêà:
îáúåì ãàçà ïðÿìî ïðîïîðöèîíàëåí åãî àáñîëþòíîé
òåìïåðàòóðå (ïðè ïîñòîÿííîé ìàññå: V = kT, ãäå k
– êîýôôèöèåíò ïðîïîðöèîíàëüíîñòè). Ýòî
ñîîòíîøåíèå çàïèñûâàåòñÿ îáû÷íî â áîëåå óäîáíîé
ôîðìå äëÿ ðåøåíèÿ çàäà÷:
Íàïðèìåð, åñëè 100 ë ãàçà, íàõîäÿùåãîñÿ ïðè
òåìïåðàòóðå 300Ê, íàãðåâàþò äî 400Ê, íå ìåíÿÿ
äàâëåíèÿ, òî ïðè áîëåå âûñîêîé òåìïåðàòóðå íîâûé
îáúåì ãàçà áóäåò ðàâåí
Çàïèñü îáúåäèíåííîãî ãàçîâîãî çàêîíà pV/T= = const
ìîæåò áûòü ïðåîáðàçîâàíà â óðàâíåíèå
Ìåíäåëååâà-Êëàïåéðîíà:
ãäå R – óíèâåðñàëüíàÿ ãàçîâàÿ ïîñòîÿííàÿ, a – ÷èñëî ìîëåé
ãàçà.
Óðàâíåíèå Ìåíäåëååâà-Êëàïåéðîíà ïîçâîëÿåò
ïðîâîäèòü ñàìûå ðàçíîîáðàçíûå âû÷èñëåíèÿ.
Íàïðèìåð, ìîæíî îïðåäåëèòü ÷èñëî ìîëåé ãàçà ïðè
äàâëåíèè 3 àòì è òåìïåðàòóðå 400Ê, çàíèìàþùèõ îáúåì
70 ë:
Îäíî èç ñëåäñòâèé îáúåäèíåííîãî ãàçîâîãî
çàêîíà: â ðàâíûõ îáúåìàõ ðàçëè÷íûõ ãàçîâ ïðè
îäèíàêîâîé òåìïåðàòóðå è äàâëåíèè ñîäåðæèòñÿ
îäèíàêîâîå ÷èñëî ìîëåêóë. Ýòî çàêîí Àâîãàäðî.
Èç çàêîíà Àâîãàäðî â ñâîþ î÷åðåäü âûòåêàåò
òàêæå âàæíîå ñëåäñòâèå: ìàññû äâóõ îäèíàêîâûõ
îáúåìîâ ðàçëè÷íûõ ãàçîâ (åñòåñòâåííî, ïðè
îäèíàêîâûõ äàâëåíèè è òåìïåðàòóðå) îòíîñÿòñÿ êàê
èõ ìîëåêóëÿðíûå ìàññû:
m1/m2 = M1/M2
(m1è m2 – ìàññû äâóõ ãàçîâ);
M1IM2ïðåäñòàâëÿåò ñîáîé
îòíîñèòåëüíóþ ïëîòíîñòü.
Çàêîí Àâîãàäðî ïðèìåíèì òîëüêî ê èäåàëüíûì
ãàçàì. Ïðè íîðìàëüíûõ óñëîâèÿõ òðóäíî ñæèìàåìûå
ãàçû (âîäîðîä, ãåëèé, àçîò, íåîí, àðãîí) ìîæíî
ñ÷èòàòü èäåàëüíûìè. Ó îêñèäà óãëåðîäà (IV),
àììèàêà, îêñèäà ñåðû (IV) îòêëîíåíèÿ îò
èäåàëüíîñòè íàáëþäàþòñÿ óæå ïðè íîðìàëüíûõ
óñëîâèÿõ è âîçðàñòàþò ñ ðîñòîì äàâëåíèÿ è
ïîíèæåíèåì òåìïåðàòóðû.
Ïðèìåð 1. Óãëåêèñëûé ãàç îáúåìîì 1 ë ïðè
íîðìàëüíûõ óñëîâèÿõ èìååò ìàññó 1,977 ã. Êàêîé
ðåàëüíûé îáúåì çàíèìàåò ìîëü ýòîãî ãàçà (ïðè í.
ó.)? Îòâåò ïîÿñíèòå.
Ðåøåíèå. Ìîëÿðíàÿ ìàññà Ì (CO2)
= 44 ã/ìîëü, òîãäà îáúåì ìîëÿ 44/1,977 = 22,12 (ë). Ýòà
âåëè÷èíà ìåíüøå ïðèíÿòîé äëÿ èäåàëüíûõ ãàçîâ
(22,4 ë). Óìåíüøåíèå îáúåìà ñâÿçàíî ñ âîçðàñòàíèåì
âçàèìî äåéñòâèÿ ìåæäó ìîëåêóëàìè ÑÎ2, ò. å.
îòêëîíåíèåì îò èäåàëüíîñòè.
Ïðèìåð 2. Ãàçîîáðàçíûé õëîð ìàññîé 0,01 ã,
íàõîäÿùèéñÿ â çàïàÿííîé àìïóëå îáúåìîì 10 ñì3,
íàãðåâàþò îò 0 äî 273oÑ. ×åìó ðàâíî íà÷àëüíîå
äàâëåíèå õëîðà ïðè 0oÑ è ïðè 273oÑ?
Ðåøåíèå. Ìr(Ñl2) =70,9; îòñþäà 0,01 ã
õëîðà ñîîòâåòñòâóåò 1,4 10-4
ìîëü. Îáúåì àìïóëû ðàâåí 0,01 ë. Èñïîëüçóÿ
óðàâíåíèå Ìåíäåëååâà-Êëàïåéðîíà pV=vRT, íàõîäèì
íà÷àëüíîå äàâëåíèå õëîðà (p1) ïðè 0oÑ:
àíàëîãè÷íî íàõîäèì äàâëåíèå õëîðà (ð2)ïðè
273oÑ: ð2 = 0,62 àòì.
Ïðèìåð 3. ×åìó ðàâåí îáúåì, êîòîðûé çàíèìàþò 10
ã îêñèäà óãëåðîäà (II) ïðè òåìïåðàòóðå 15oÑ è
äàâëåíèè 790 ìì ðò. ñò.?
Ðåøåíèå.
Çàäà÷è
1. Êàêîé îáúåì (ïðè í. ó.) çàíèìàåò 0,5
ìîëü êèñëîðîäà?
2. Êàêîé îáúåì çàíèìàåò âîäîðîä,
ñîäåðæàùèé 18-1023 ìîëåêóë (ïðè í. ó.)?
3. ×åìó ðàâíà ìîëÿðíàÿ ìàññà îêñèäà
ñåðû(IV), åñëè ïëîòíîñòü ýòîãî ãàçà ïî âîäîðîäó
ðàâíà 32?
4. Êàêîé îáúåì çàíèìàþò 68 ã àììèàêà ïðè
äàâëåíèè 2 àòì è òåìïåðàòóðå 100oÑ?
5. Â çàìêíóòîì ñîñóäå åìêîñòüþ 1,5 ë
íàõîäèòñÿ ñìåñü ñåðîâîäîðîäà ñ èçáûòêîì
êèñëîðîäà ïðè òåìïåðàòóðå 27oÑ è äàâëåíèè
623,2 ìì ðò. ñò. Íàéäèòå ñóììàðíîå êîëè÷åñòâî
âåùåñòâ â ñîñóäå.
6. Â áîëüøîì ïîìåùåíèè òåìïåðàòóðà ìîæåò
èçìåðÿòüñÿ ñ ïîìîùüþ “ãàçîâîãî” òåðìîìåòðà.
Äëÿ ýòîé öåëè ñòåêëÿííóþ òðóáêó, èìåþùóþ
âíóòðåííèé îáúåì 80 ìë, çàïîëíèëè àçîòîì ïðè
òåìïåðàòóðå 20oÑ è äàâëåíèè 101,325 êÏà. Ïîñëå
ýòîãî òðóáêó ìåäëåííî è îñòîðîæíî âûíåñëè èç
êîìíàòû â áîëåå òåïëîå ïîìåùåíèå. Áëàãîäàðÿ
òåðìè÷åñêîìó ðàñøèðåíèþ, ãàç âûøåë èç òðóáêè è
áûë ñîáðàí íàä æèäêîñòüþ, äàâëåíèå ïàðà êîòîðîé
íåçíà÷èòåëüíî. Îáùèé îáúåì ãàçà, âûøåäøåãî èç
òðóáêè (èçìåðåí ïðè 20oÑ è 101,325 êÏà), ðàâåí 3,5
ìë. Ñêîëüêî ìîëåé àçîòà ïîòðåáîâàëîñü äëÿ
çàïîëíåíèÿ ñòåêëÿííîé òðóáêè è êàêîâà
òåìïåðàòóðà áîëåå òåïëîãî ïîìåùåíèÿ?
7. Õèìèê, îïðåäåëÿâøèé àòîìíóþ ìàññó
íîâîãî ýëåìåíòà X â ñåðåäèíå XIX â., âîñïîëüçîâàëñÿ
ñëåäóþùèì ìåòîäîì: îí ïîëó÷àë ÷åòûðå ñîåäèíåíèÿ,
ñîäåðæàùèå ýëåìåíò X (À, Á, Â è Ã), è îïðåäåëÿë
ìàññîâóþ äîëþ ýëåìåíòà (%) â êàæäîì èç íèõ. Â ñîñóä,
èç êîòîðîãî ïðåäâàðèòåëüíî áûë îòêà÷àí âîçäóõ,
îí ïîìåùàë êàæäîå ñîåäèíåíèå, ïåðåâåäåííîå â
ãàçîîáðàçíîå ñîñòîÿíèå ïðè 250oÑ, è
óñòàíàâëèâàë ïðè ýòîì äàâëåíèå ïàðîâ âåùåñòâà
1,013 105 Ïà. Ïî
ðàçíîñòè ìàññ ïóñòîãî è ïîëíîãî ñîñóäîâ
îïðåäåëÿëàñü ìàññà ãàçîîáðàçíîãî âåùåñòâà.
Àíàëîãè÷íàÿ ïðîöåäóðà ïðîâîäèëàñü ñ àçîòîì. Â
ðåçóëüòàòå ìîæíî áûëî ñîñòàâèòü òàêóþ òàáëèöó:
| Ãàç | Îáùàÿ ìàññà, ã | Ìàññîâàÿ äîëÿ () ýëåìåíòà x â âåùåñòâå, % |
| N2 | 0,652 | – |
| À | 0,849 | 97,3 |
| Á | 2,398 | 68,9 |
| Â | 4,851 | 85,1 |
| Ã | 3,583 | 92,2 |
Îïðåäåëèòå âåðîÿòíóþ àòîìíóþ ìàññó ýëåìåíòà X.
8. Â 1826 ã. ôðàíöóçñêèé õèìèê Äþìà
ïðåäëîæèë ìåòîä îïðåäåëåíèÿ ïëîòíîñòè ïàðîâ,
ïðèìåíèìûé êî ìíîãèì âåùåñòâàì. Ïî ýòîìó ìåòîäó
ìîæíî áûëî íàõîäèòü ìîëåêóëÿðíûå ìàññû
ñîåäèíåíèé, èñïîëüçóÿ ãèïîòåçó Àâîãàäðî î òîì,
÷òî â ðàâíûõ îáúåìàõ ãàçîâ è ïàðîâ ïðè ðàâíîì
äàâëåíèè è òåìïåðàòóðå ñîäåðæàòñÿ îäèíàêîâûå
êîëè÷åñòâà ìîëåêóë. Îäíàêî ýêñïåðèìåíòû ñ
íåêîòîðûìè âåùåñòâàìè, ñäåëàííûå ïî ñïîñîáó
Äþìà, ïðîòèâîðå÷èëè ãèïîòåçå Àâîãàäðî è ñòàâèëè
ïîä ñîìíåíèå ñàìó âîçìîæíîñòü îïðåäåëåíèÿ
ìîëåêóëÿðíîé ìàññû äàííûì ñïîñîáîì. Âîò îïèñàíèå
îäíîãî èç òàêèõ ýêñïåðèìåíòîâ (ðèñ. 2).
à. Â ãîðëûøêå ñîñóäà à èçâåñòíîãî îáúåìà
ïîìåñòèëè íàâåñêó íàøàòûðÿ á è íàãðåëè â ïå÷è â äî
òàêîé òåìïåðàòóðû to, ïðè êîòîðîé âåñü
íàøàòûðü èñïàðèëñÿ. Ïîëó÷èâøèåñÿ ïàðû âûòåñíèëè
âîçäóõ èç ñîñóäà, ÷àñòü èõ âûäåëèëàñü íàðóæó â
âèäå òóìàíà. Íàãðåòûé äî toñîñóä,
äàâëåíèå â êîòîðîì ðàâíÿëîñü àòìîñôåðíîìó,
çàïàÿëè ïî ïåðåòÿæêå ã, çàòåì îõëàäèëè è
âçâåñèëè.
Çàòåì ñîñóä âñêðûëè, îòìûëè îò
ñêîíäåíñèðîâàííîãî íàøàòûðÿ, âûñóøèëè è ñíîâà
âçâåñèëè. Ïî ðàçíîñòè îïðåäåëèëè ìàññó m
íàøàòûðÿ.
Ýòà ìàññà ïðè íàãðåâàíèè äî toèìåëà
äàâëåíèå ð, ðàâíîå àòìîñôåðíîìó, â ñîñóäå
îáúåìîì V. Äëÿ ñîñóäà à çàðàíåå áûëè
îïðåäåëåíû äàâëåíèå è îáúåì èçâåñòíîé ìàññû
âîäîðîäà ïðè êîìíàòíîé òåìïåðàòóðå. Îòíîøåíèå
ìîëåêóëÿðíîé ìàññû íàøàòûðÿ ê ìîëåêóëÿðíîé
ìàññå âîäîðîäà îïðåäåëÿëè ïî ôîðìóëå
Ïîëó÷èëè âåëè÷èíó Ì/Ì(Í2) = 13,4.
Îòíîøåíèå, âû÷èñëåííîå ïî ôîðìóëå NH4Cl,
ñîñòàâèëî 26,8.
á. Îïûò ïîâòîðèëè, íî ãîðëûøêî ñîñóäà çàêðûëè
ïîðèñòîé àñáåñòîâîé ïðîáêîé ä, ïðîíèöàåìîé
äëÿ ãàçîâ è ïàðîâ. Ïðè ýòîì ïîëó÷èëè îòíîøåíèå Ì
/Ì(Í2) = 14,2.
â. Ïîâòîðèëè îïûò á, íî óâåëè÷èëè íà÷àëüíóþ
íàâåñêó íàøàòûðÿ â 3 ðàçà. Îòíîøåíèå ñòàëî ðàâíûì
Ì/Ì (Í2) = 16,5.
Îáúÿñíèòå ðåçóëüòàòû îïèñàííîãî ýêñïåðèìåíòà è
äîêàæèòå, ÷òî çàêîí Àâîãàäðî â äàííîì ñëó÷àå
ñîáëþäàëñÿ.
Ðåøåíèÿ
1. Ìîëü ëþáîãî ãàçà çàíèìàåò îáúåì (ïðè í. ó.) 22,4 ë;
0,5 ìîëü Î2 çàíèìàåò îáúåì 22,40,5 = 11,2 (ë).
2. ×èñëî ìîëåêóë âîäîðîäà, ðàâíîå 6,02-1023
(÷èñëî Àâîãàäðî), ïðè í. ó. çàíèìàåò îáúåì 22,4 ë (1
ìîëü); òîãäà
3. Ìîëÿðíàÿ ìàññà îêñèäà cepû(IV) : M(SO2) = 322 = 64 (ã/ìîëü).
4. Ïðè í. ó. 1 ìîëü NÍç, ðàâíûé 17 ã, çàíèìàåò îáúåì 22,4
ë, 68 ã çàíèìàåò îáúåì õ ë,
Èç óðàâíåíèÿ ãàçîâîãî ñîñòîÿíèÿ poVo/To
= p1V1/T1 íàõîäèì
5.
ñìåñè H2S
è Î2.
6. Ïðè çàïîëíåíèè òðóáêè àçîòîì
 òðóáêå îñòàëîñü (ïðè íà÷àëüíûõ óñëîâèÿõ) V1:
80-3,5 = 76,5 (ìë). Ïðè ïîâûøåíèè òåìïåðàòóðû àçîò,
çàíèìàâøèé îáúåì 76,5 ìë (V1) ïðè 20oÑ,
ñòàë çàíèìàòü îáúåì V2 = 80 ìë. Òîãäà, ñîãëàñíî
Ò1/Ò2= = V1/V2 èìååì
Ïðåäïîëîæèì, ÷òî ïðè òåìïåðàòóðå 250î
Ñ âåùåñòâà À, Á, Â, Ã ÿâëÿþòñÿ èäåàëüíûìè ãàçàìè.
Òîãäà ïî çàêîíó Àâîãàäðî
Ìàññà ýëåìåíòà X â 1 ìîëü âåùåñòâà À, Á, Â è Ã
(ã/ìîëü):
Ì(À) .0,973 = 35,45; Ì(Á) .0,689 = 70,91; Ì (Â).0,851
= 177,17; Ì(Ã).0,922= 141,78
Ïîñêîëüêó â ìîëåêóëå âåùåñòâà äîëæíî áûòü
öåëîå ÷èñëî àòîìîâ ýëåìåíòà X, íóæíî íàéòè
íàèáîëüøèé îáùèé äåëèòåëü ïîëó÷åííûõ âåëè÷èí. Îí
ñîñòàâëÿåò 35,44 ã/ìîëü, è ýòî ÷èñëî ìîæíî ñ÷èòàòü
âåðîÿòíîé àòîìíîé ìàññîé ýëåìåíòà X.
8. Îáúÿñíèòü ðåçóëüòàòû ýêñïåðèìåíòà ëåãêî
ñóìååò ëþáîé ñîâðåìåííûé õèìèê. Õîðîøî èçâåñòíî,
÷òî âîçãîíêà íàøàòûðÿ – õëîðèäà àììîíèÿ –
ïðåäñòàâëÿåò ñîáîé îáðàòèìûé ïðîöåññ
òåðìè÷åñêîãî ðàçëîæåíèÿ ýòîé ñîëè:
| NH4Cl | NH3 | + HCl. | |
| 53,5 | 17 | 36,5 |
 ãàçîâîé ôàçå íàõîäÿòñÿ àììèàê è õëîðîâîäîðîä,
èõ ñðåäíÿÿ îòíîñèòåëüíàÿ ìîëåêóëÿðíàÿ ìàññà Ìò
Ìåíåå ïîíÿòíî èçìåíåíèå ðåçóëüòàòà ïðè
íàëè÷èè àñáåñòîâîé ïðîáêè. Îäíàêî â ñåðåäèíå
ïðîøëîãî âåêà èìåííî îïûòû ñ ïîðèñòûìè
(“ñêâàæèñòûìè”) ïåðåãîðîäêàìè ïîêàçàëè, ÷òî
â ïàðàõ íàøàòûðÿ ñîäåðæàòñÿ äâà ãàçà. Áîëåå
ëåãêèé àììèàê ïðîõîäèò ñêâîçü ïîðû áûñòðåå, è åãî
ëåãêî çàìåòèòü ëèáî ïî çàïàõó, ëèáî ñ ïîìîùüþ
âëàæíîé èíäèêàòîðíîé áóìàãè.
Ñòðîãîå âûðàæåíèå äëÿ îöåíêè îòíîñèòåëüíîé
ïðîíèöàåìîñòè ãàçîâ ñêâîçü ïîðèñòûå ïåðåãîðîäêè
äàåò ìîëåêóëÿðíî-êèíåòè÷åñêàÿ òåîîèÿ ãàçîâ.
Ñðåäíÿÿ ñêîðîñòü ìîëåêóë ãàçà
, ãäå R – ãàçîâàÿ
ïîñòîÿííàÿ; Ò – àáñîëþòíàÿ òåìïåðàòóðà; Ì
– ìîëÿðíàÿ ìàññà. Ïî ýòîé ôîðìóëå àììèàê äîëæåí
äèôôóíäèðîâàòü áûñòðåå õëîðîâîäîðîäà:
Ñëåäîâàòåëüíî, ïðè ââåäåíèè â ãîðëî êîëáû
àñáåñòîâîé ïðîáêè ãàç â êîëáå óñïååò íåñêîëüêî
îáîãàòèòüñÿ òÿæåëûì ÍÑ1 çà âðåìÿ, ïîêà ïðîèñõîäèò
âûðàâíèâàíèå äàâëåíèÿ ñ àòìîñôåðíûì.
Îòíîñèòåëüíàÿ ïëîòíîñòü ãàçà ïðè ýòîì
âîçðàñòàåò. Ïðè óâåëè÷åíèè ìàññû NH4C1
äàâëåíèå, ðàâíîå àòìîñôåðíîìó, óñòàíîâèòñÿ ïîçæå
(àñáåñòîâàÿ ïðîáêà ïðåïÿòñòâóåò áûñòðîìó
âûòåêàíèþ ïàðîâ èç êîëáû), ãàç â êîëáå áóäåò
ñîäåðæàòü õëîðîâîäîðîäà áîëüøå, ÷åì â ïðåäûäóùåì
ñëó÷àå; ïëîòíîñòü ãàçà óâåëè÷èòñÿ.
Источник
Решениие задач по химии на закон Авогадро
Задача 53.
Сопоставить числа молекул, содержащихся в 1г NH3 и в 1г N2. В каком случае и во сколько раз число молекул больше?
Решение:
В одном моле любого вещества содержится 6,02 . 1023 молекул этого вещества.
Рассчитаем содержание количества вещества в 1г NH3 и N2 по формуле:
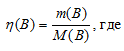
 (B) – количество вещества (В);
(B) – количество вещества (В);
m(B)- масса вещества (В);
M(B) – Молярная масса вещества (В).
М(NH3) = 17г/моль, M(N2) = 28г/моль.
Тогда
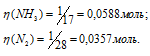
Число молекул NH3 больше числа молекул N2, так как  (NH3) >
(NH3) > (N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
(N2) . Теперь рассчитаем, во сколько раз число молекул NH3 больше числа молекул N2:
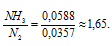
Ответ: в 1,65 раз число молекул NH3 больше числа молекул N2.
Задача 54.
Выразить в граммах массу одной молекулы диоксида серы.
Решение:
Находим молекулярную массу диоксида серы:
M(SO2) = 32 + (16 . 2) = 64г/моль.
Молекулярная масса численно составляет массу одного моля вещества, а значит, вес одного моля численно равен молекулярной массе и составляет 64г. Известно, что в одном моле любого вещества содержится 6,02 . 1023 молекул данного вещества. Исходя из этого, рассчитаем массу в граммах одной молекулы диоксида серы:
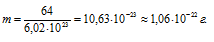
Ответ: масса одной молекулы диоксида серы равна.
Задача 55.
Одинаково ли число молекул в 0,001кг Н2 и в 0,001кг О2? В 1 моле Н2 и в 1 моле 02? В 1л Н2 и в 1л О2 при одинаковых условиях?
Решение:
Молекулярные массы водорода и кислорода равны соответственно 2г/моль и 32г/моль. Отсюда находим количество водорода и кислорода, зная их массы:
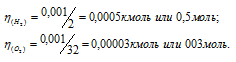
Один моль любого вещества содержит 6,02 .1023 молекул. Следовательно, в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул:

Так как имеется по одному молю водорода и кислорода, то количество молекул веществ будет одинаково:
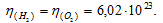
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1л водорода и в 1л кислорода:
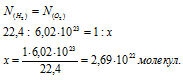
Ответ: а) в 0,001кг водорода и в 0,001кг кислорода содержится разное число молекул; б) в одном моле водорода и в одном моле кислорода содержится одинаковое число молекул: в) в одном литре водорода и в одном литре кислорода содержится одинаковое число молекул.
Задача 56.
Сколько молекул содержится в 1,00 мл водорода при нормальных условиях?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 .1023 молекул. Отсюда рассчитаем количество молекул вещества, содержащихся в 1мл водорода из пропорции:
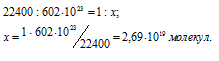
Ответ: 2,69 .1019 молекул.
Задача 57.
Какой объем при нормальных условиях занимают 27 .1021 молекул газа?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л, В которых содержится 6,02 . 1023 молекул. Отсюда находим какой объём при нормальных условиях занимают 27 .1021 молекул газа, составив пропорцию:
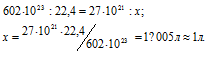
Ответ: V=1л.
Задача 58.
Каково соотношение объемов, занимаемых 1 молем О2 и 1 молем О3 (условия одинаковые)?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Следовательно соотношение объёмов, занимаемых одним молем О2 и одним молем О3 иметь вид:
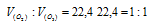
Ответ: 1:1
Задача 59.
Взяты равные массы кислорода, водорода и метана при одинаковых условиях. Найти отношение объемов взятых газов.
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Мольные массы кислорода, водорода и метана, соответственно равны 32 г/моль; 2г/моль; 16 г/моль.
Так как массы кислорода, водорода и метана одинаковы при одинаковых условиях, то отношение объёмов взятых газов находим из пропорции:
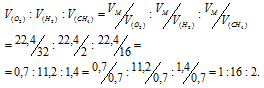
Ответ: 1:16:2.
Задача 60.
На вопрос, какой объем займет 1моль воды при нормальных условиях, получен ответ: 22,4л. Правильный ли это ответ?
Решение:
Согласно закону Авогадро в равных объёмах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул, Один моль любого газа занимает 22,4л. Так как вода при нормальных условиях находится в жидкой, а не в газообразной фазе, то ответ, что 1моль воды займёт 22,4л не правильный. Учитывая, что молярная масса воды равна 18г/моль, а плотность равна единице, то правильный ответ будет равен:
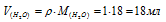
Ответ: 18мл.
Задача 61.
Сколько молекул диоксида углерода находится в 1л воздуха, если объемное содержание СО2 составляет 0,03% (условия нормальные)?
Решение:
При нормальных условиях углекислый газ, содержащийся в 1л воздуха, занимает объём 0,0003л. Зная, что мольный объём любого газа занимает 22,4л, рассчитаем число молей углекислого газа в 0,0003л из пропорции:
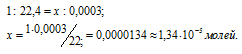
Учитывая, что в одном моле вещества содержится 6,02 . 1023 молекул, находим число молекул в 0,0003л газа:

Ответ: 8,07 .1018 молекул.
Источник
