В сосуде вместимостью 224 л при нормальных условиях

- Главная
- Вопросы & Ответы
- Вопрос 2766439
более месяца назад
Просмотров : 171
Ответов : 1
Лучший ответ:

M=m:v=40:(224:22.4)=4.Газ с молярной m-гелийHE
более месяца назад
Ваш ответ:
Комментарий должен быть минимум 20 символов
Чтобы получить баллы за ответ войди на сайт

Лучшее из галереи за : неделю месяц все время































Другие вопросы:
На бревне массой 100 кг. сидят три друга. Длина бревна 3метра. Первый друг массой 60 кг сидит на расстоянии 1 м от левого края бревна. Второй друг сидит на расстоянии 1.5 м от левого края, его масса 65 кг. Третий друг, массой 70 кг сидит на расстоянии 2м от левого края бревна.Где нужно подпереть бр…
более месяца назад
Смотреть ответ
Просмотров : 13
Ответов : 1
Установите соответствие между исходными веществами и сокращённым ионным уравнением.Исходные вещества Сокращённое ионное уравнение реакцииA)Fe2O3 HCl=FeCl3 H2O 1) Fe(OH)2 2H( ) = Fe(2 ) H2OБ)FeCl3 KOH=Fe(OH)3 KCl 2)Fe2O3 6H( )=2Fe(3 ) 3H2OВ) Fe(OH)2 H2SO4=FeSO4 H2O 3) Fe(2 ) 2OH(-)=Fe(OH)24)K( )…
более месяца назад
Смотреть ответ
Просмотров : 108
Ответов : 1
Чем было вызвано нежелание наполеона отступать по старой смоленской дороги?
более месяца назад
Смотреть ответ
Просмотров : 18
Ответов : 1
Слова с корнем лёт как минимум 10слов
более месяца назад
Смотреть ответ
Просмотров : 21
Ответов : 1
груз весом 2500 Н поднимают с помощью неподвижного блока на высоту 2 м прикладывая усилие 2750 Н Сколько энергии преобразуется при этом в местах трения вовнутреннюю энергию?
более месяца назад
Смотреть ответ
Просмотров : 25
Ответов : 1
Источник
Задача 41.
Смешивают 0,04м3 азота, находящегося под давлением 96кПа (720мм. рт. ст.), с 0,02м3 кислорода. Общий объем смеси 0,06м3, а общее давление 97,6кПа (732мм. рт. ст.). Каким было давление взятого кислорода?
Решение:
По условию задачи объём азота увеличился в 1,5 раза (0,06/0,04 = 1,5), а объём кислорода – в 3 раза (0,06/0,02 = 3). Во столько же раз уменьшились парциальные давления газов.
Следовательно,
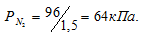
Согласно закону парциальных давлений, общее давление смеси газов, не вступающих во взаимодействие друг с другом, равно сумме парциальных давлений газов, составляющих систему (смесь). Отсюда Исходя из того, что объём кислорода до смешения был в три раза больше, чем после смешения, рассчитаем давление кислорода до смешения:
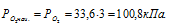
Ответ: Робщ. = 100,8кПа.
Задача 42.
Газовая смесь приготовлена из 2л Н2 (Р = 93,3 кПа) и 5л CH4 (Р = 112 кПа). Объем смеси равен 7л. Найти парциальные давления газов и общее давление смеси.
Решение:
По условию задачи объём водорода увеличился в 3,5 раза (7/2 = 3,5), а объём метана – в 1,4 раза (7/5 = 1,4). Во столько же раз уменьшились парциальные давления газов.
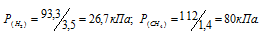
Согласно закону парциальных давлений, общее давление смеси газов, не вступающих во взаимодействие друг с другом, равно сумме парциальных давлений газов, составляющих систему (смесь).
Отсюда:
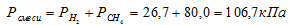
Ответ: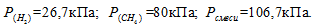
Задача 43.
Газовая смесь состоит из NO и СО2. Вычислить объемное содержание газов в смеси (в %), если их парциальные давления равны соответственно 36,3 и 70,4 кПа (272 и 528мм. рт. ст.).
Решение:
Согласно закону Дальтона парциальное давление данного газа прямо пропорционально его мольной доли на общее давление смеси газов:
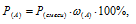
где Р(смеси) – общее давление смеси; Р(А) – парциальное давление данного газа; (A) – мольная доля данного газа.
Согласно закону парциальных давлений, общее давление смеси газов, не вступающих во взаимодействие друг с другом, равно сумме парциальных давлений газов, составляющих систему (смесь).
Отсюда:
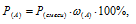
Ответ: 34,02%NO; 65,98%CO.
Задача 44.
В закрытом сосуде вместимостью 0,6м3 находится при 0 °С смесь, состоящая из 0,2кг СО2, 0,4кг 02 и 0,15кг СН4. Вычислить: а) общее давление смеси; б) парциальное давление каждого из газов; в) процентный состав смеси по объему.
Решение:
Вычислим общее количество газов в смеси по уравнению:
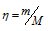 , где
, где
 – количество газа, кмоль; m – масса газа, кг; М – молекулярная масса газа, кг/моль. Тогда:
– количество газа, кмоль; m – масса газа, кг; М – молекулярная масса газа, кг/моль. Тогда:
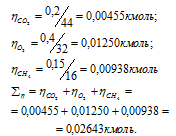
а) Общее давление смеси газов определяем по уравнению:
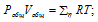
Тогда:
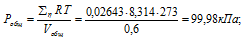
б) Парциальные давления газов рассчитываем по уравнению:
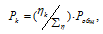
где Rk и  k , соответственно, парциальное давление, и количество газа в смеси.
k , соответственно, парциальное давление, и количество газа в смеси.
Тогда
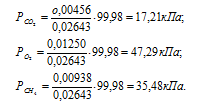
в) Парциальные объёмы газов рассчитаем по уравнению:
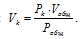
Тогда
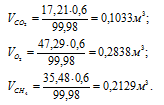
Отношение парциальных (приведённых) объёмов отдельных газов к общему объёму смеси называется объёмной долей и определяется по формуле:
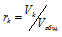
Тогда
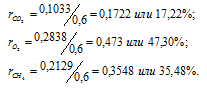
Ответ: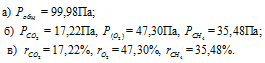
Задача 45.
Газовая смесь приготовлена из 0,03м3 СН4, 0,04м3 Н2 и 0,01м3 СО. Исходные давления СН4, Н2 и СО составляли ответственно 96, 84 и 108,8 кПа (720, 630 и 816мм рт. ст.). Объем смеси равен 0,08м3. Определить парциальные давления газов и общее давление смеси.
Решение:
По условию задачи объём метана увеличился после смешения в 2,67 раза (0,08/0,03 = 2,67), объём водорода – в 2 раза (0,08/0,04 = 2), а объём угарного газа – в 8 раз (0,08/0,01 = 8). Во столько же раз уменьшились парциальные давления газов. Следовательно,
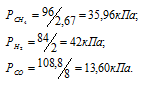
Согласно закону парциальных давлений, общее давление смеси газов, не вступающих во взаимодействие друг с другом, равно сумме парциальных давлений газов, составляющих систему (смесь).
Отсюда:
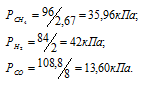
Ответ: 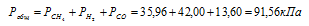
Задача 46.
В газометре над водой находятся 7,4л кислорода при 23 °С и давлении 104,1 кПа (781 мм. рт. ст.). Давление насыщенного водяного пара при 23 °С равно 2,8 кПа (21мм. рт. ст.). Какой объем займет находящийся в газометре кислород при нормальных условиях?
Решение:
Парциальное давление кислорода равно разности общего давления и парциального давления паров воды:
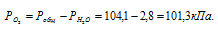
Обозначив искомый объём через и, используя объединённое уравнение закона Бойля- Мариотта и Гей-Люссака, находим:
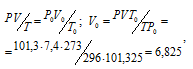
где Р и V – давление и объём газа при температуре Т = 296К (273 +23 = 296); Р0 = 101,325кПа; Т0 = 273К; Р = 104,1кПа; – объём газа при н.у.
Ответ: V0 =6,825л.
Источник
