В закрытом сосуде 2 находится 280 азота
Опубликовано 10 месяцев назад по предмету
Физика
от yaa19
Ответ
Ответ дан
yaa19спасибо большое!
Не тот ответ, который вам нужен?
Найди нужный
Самые новые вопросы
![]()
Математика – 6 месяцев назад
Сколько здесь прямоугольников
![]()
История – 1 год назад
Какое управление было в древнейшем риме? как звали первого и последнего из царей рима?
![]()
Литература – 1 год назад
Уроки французского ответе на вопрос : расскажите о герое по следующему примерному плану: 1.почему мальчик оказался в райцентре ? 2.как он чувствовал себя на новом месте? 3.почему он не убежал в деревню? 4.какие отношения сложились у него с товарищами? 5.почему он ввязался в игру за деньги? 6.как характеризуют его отношения с учительницей ? ответе на эти вопросы пожалуйста ! сочините сочинение пожалуйста
![]()
Русский язык – 1 год назад
Помогите решить тест по русскому языку тест по русскому языку «местоимение. разряды местоимений» для 6 класса
1. укажите личное местоимение:
1) некто
2) вас
3) ни с кем
4) собой
2. укажите относительное местоимение:
1) кто-либо
2) некоторый
3) кто
4) нам
3. укажите вопросительное местоимение:
1) кем-нибудь
2) кем
3) себе
4) никакой
4. укажите определительное местоимение:
1) наш
2) который
3) некий
4) каждый
5. укажите возвратное местоимение:
1) свой
2) чей
3) сам
4) себя
6. найдите указательное местоимение:
1) твой
2) какой
3) тот
4) их
7. найдите притяжательное местоимение:
1) самый
2) моего
3) иной
4) ничей
8. укажите неопределённое местоимение:
1) весь
2) какой-нибудь
3) любой
4) этот
9. укажите вопросительное местоимение:
1) сколько
2) кое-что
3) она
4) нами
10. в каком варианте ответа выделенное слово является притяжательным местоимением?
1) увидел их
2) её нет дома
3) её тетрадь
4) их не спросили
![]()
Русский язык – 1 год назад
Переделай союзное предложение в предложение с бессоюзной связью.
1. океан с гулом ходил за стеной чёрными горами, и вьюга крепко свистала в отяжелевших снастях, а пароход весь дрожал.
2. множество темноватых тучек, с неясно обрисованными краями, расползались по бледно-голубому небу, а довольно крепкий ветер мчался сухой непрерывной струёй, не разгоняя зноя
3. поезд ушёл быстро, и его огни скоро исчезли, а через минуту уже не было слышно шума
![]()
Русский язык – 1 год назад
помогите прошу!перепиши предложения, расставляя недостающие знаки препинания. объясни, что соединяет союз и. если в предложении один союз и, то во втором выпадающем списке отметь «прочерк».пример:«я шёл пешком и,/поражённый прелестью природы/, часто останавливался».союз и соединяет однородные члены.ночь уже ложилась на горы (1) и туман сырой (2) и холодный начал бродить по ущельям.союз и соединяет:1) части сложного предложенияоднородные члены,2) однородные членычасти сложного предложения—.поэт — трубач зовущий войско в битву (1) и прежде всех идущий в битву сам (ю. янонис).союз и соединяет:1) части сложного предложенияоднородные члены,2)
![]()
Физика – 1 год назад
Вокруг прямого проводника с током (смотри рисунок) существует магнитное поле. определи направление линий этого магнитного поля в точках a и b.обрати внимание, что точки a и b находятся с разных сторон от проводника (точка a — снизу, а точка b — сверху). рисунок ниже выбери и отметь правильный ответ среди предложенных.1. в точке a — «от нас», в точке b — «к нам» 2. в точке a — «к нам», в точке b — «от нас» 3. в обеих точках «от нас»4. в обеих точках «к нам»контрольная работа по физике.прошу,не наугад важно
Информация
Посетители, находящиеся в группе Гости, не могут оставлять комментарии к данной публикации.
Источник
Spbmasha123 / 22 дек. 2013 г., 4:15:34
кг/м3
2) 0,9 кг/м3
3) 0,225 кг/м3
4) 111 кг/м3
Сравните плотности веществ, из которых изготовлены кубики 1 и 2.
1) ρ1 >ρ2
2) ρ1 =ρ2
3) ρ1 <ρ2
4)плотности сравнить нельзя
В ядре натрия 23 частицы. Из них 12 нейтронов. Сколько в ядре протонов?
1)11 протонов
2) 35 протонов
3) 10 протонов
4) 23 протона
Давлением называют величину, равную:
1) отношению силы, действующей перпендикулярно поверхности, к площади этой поверхности
2) произведение силы, действующей перпендикулярно поверхности, и площади этой поверхности
3) отношение площади поверхности к силе, действующей перпендикулярно этой поверхности
4) произведению квадрата силы, действующей перпендикулярно поверхности, и площади этой поверхности
Какое физическое явление лежит в основе устройства и работы ртутного термометра?
1) плавление твердого тела при нагревании
2) конвекция в жидкости при нагревании
3) расширение жидкости при нагревании
4) испарение жидкости
Укажите верные окончания для фраз:
Температура кипения жидкости…
а) с ростом атмосферного давления увеличивается
Температура испарения жидкости…
б) с ростом атмосферного давления уменьшается
Температура конденсации жидкости…
в) не зависит от атмосферного давления
1) а, в, а
2)а, б, а
3)а, а, а
4)б, в, в
Как изменяется внутренняя энергия вещества при переходе из твердого состояния в жидкое при постоянной температуре?
1) у разных веществ изменяется по-разному
2) может увеличиваться или уменьшаться в зависимости от внешних условий
3) остается постоянной
4) увеличивается
Какой физический параметр определяет количество теплоты, необходимое для превращения 1 кг жидкости в пар при температуре кипения?
1)удельная теплота сгорания
2) удельная теплота парообразования
3) удельная теплота плавления
4) удельная теплоемкость
Внутренняя энергия стального шарика изменится, если:
1) поднять его над землей;
2) бросить его горизонтально;
3) сильно ударить по нему молотком;
4) изменить нельзя.
Какая скорость больше: 20 м/с или 72 км/ч?
1) 20 м/с;
2) 72 км/ч;
3) они равны;
4) определить невозможно.
В каком варианте ответа правильно указан порядок пропущенных в предложении слов?
Протоны имеют… заряд, а нейтроны…
1) положительный, отрицательный;
2) положительный, заряда не имеют;
3) отрицательный, положительный;
4) отрицательный, заряда не имеют.
Что является причиной возникновения силы трения?
1) шероховатость поверхностей соприкасающихся тел;
2) взаимное притяжение молекул соприкасающихся тел;
3) шероховатость поверхностей или взаимное притяжение молекул соприкасающихся тел;
4) среди ответов 1-3 нет правильного.
Вода начала превращаться в лед. При дальнейшей кристаллизации ее температура:
1) будет увеличиваться;
2) будет уменьшаться;
3) не будет изменяться;
4) сначала увеличится, затем уменьшится.
Единица электрического сопротивления – это:
1) 1 Кл; 2) 1 Ом; 3) 1 А; 4) 1 В.
Электрическое напряжение вычисляется по формуле:
1) U = R/I; 2) U = I/R; 3) U = I R; 4) I = U/R.
Сила тока в цепи уменьшится, если:
1) напряжение повысится;
2) напряжение понизится;
3) сопротивление уменьшится;
4) сила тока не зависит от напряжения и сопротивления.
Как изменится давление, если силу давления увеличить в 2 раза, а площадь уменьшить в 2 раза?
1) уменьшится в 4 раза; 2) уменьшится в 2 раза;
3) увеличится в 2 раза; 4) увеличится в 4 раза.
Внутренняя энергия тел зависит от:
1) скорости тела;
2) температуры тела;
3) формы тела;
4) объема тела.
Вид движения поезда при подходе к станции:
1) свободное падение;
2) замедление;
3) ускоренное;
4) равномерное.
Какие из перечисленных веществ обладают наименьшей теплопроводностью?
1) твердые; 2) жидкие;
3) газообразные; 4) твердые и жидкие.
Во вложении есть все…
Источник
Страница 1 из 2
46. Азот массой m = 10 г находится при температуре Т = 290 К. Определите: 1) среднюю кинетическую энергия одной молекулы азота; 2) среднюю кинетическую энергию вращательного движения всех молекул азота. Газ считайте идеальным.
47. Кислород массой m = 1 кг находится при температуре Т = 320 К. Определите: 1) кинетическую энергию вращательного движения молекул кислорода; 2) внутреннюю энергию молекул кислорода. Газ считайте идеальным.
48. В закрытом сосуде находится смесь азота массой m1= 56 г и кислорода массой m2 = 64 г. Определите изменение внутренней энергии этой смеси, если ее охладили на 20 °С.
49. Считая азот идеальным газом, определите его удельную теплоемкость: 1) для изохорного процесса; 2) для изобарного процесса.
50. Определите удельные теплоемкости сv и ср, если известно, что некоторый газ при нормальных условиях имеет удельный объем v = 0,7 м3/кг. Какой это газ?
51. Определите удельные теплоемкости сv и ср смеси углекислого газа массой m1 = 3 г и азота массой m2 = 4 г.
52. Определите показатель адиабаты γ для смеси газов, содержащей гелий массой m1 = 8 г и водород массой m2 = 2 г.
53. Применяя первое начало термодинамики и уравнение состояния идеального газа, покажите, что разность удельных теплоемкостей c = cp – cv = R/M.
54. Кислород массой 32 г находится в закрытом сосуде под давлением 0,1 МПа при температуре 290 К. После нагревания давление в сосуде повысилось в 4 раза. Определите: 1) объем сосуда; 2) температуру, до которой газ нагрели; 3) количество теплоты, сообщенное газом.
55. Определите количество теплоты, сообщенное газу, если в процессе изохорного нагревания кислорода объемом V = 20 л его давление изменилось на Δp = 100 кПа.
56. Двухатомный идеальный газ (ν = 2 моль) нагревают при постоянном объеме до температуры 289 К. Определите количество теплоты, которое необходимо сообщить газу, чтобы увеличить его давление в n= 3 раза.
57. При изобарном нагревании некоторого идеального газа (ν = 2 моль) на ΔT = 90 К ему было сообщено количество теплоты 5,25 кДж. Определите: 1) работу, совершаемую газом; 2) изменение внутренней энергии газа; 3) величину γ = cp/cV .
58. Азот массой m = 280 г расширяется в результате изобарного процесса при давлении p = 1 МПа. Определите: 1) работу расширения 2) конечный объем газа, если на расширение затрачена теплота Q = 5 кДж, а начальная температура азота T1 = 290 К.
59. Кислород объемом 1 л находится под давлением 1 МПа. Определите, какое количество теплоты необходимо сообщить газу, чтобы: 1) увеличить его объем вдвое в результате изобарного процесса; 2) увеличить его давление вдвое в результате изохорного процесса.
60. Некоторый газ массой m = 5 г расширяется изотермически от объема V1до объема V2 = 2V1. Работа расширения A= 1 кДж. Определите среднюю квадратичную скорость молекул газа.
61. Азот массой m = 14 г сжимают изотермически при температуре T = 300 К от давления p1 = 100 кПа до давления p2= 500 кПа. Определите: 1) изменение внутренней энергии газа; 2) работу сжатия; 3) количество выделившейся теплоты.
62. Некоторый газ массой 1 кг находится при температуре Т = 300 К и под давлением p1 = 0.5 МПа. В результате изотермического сжатия давление газа увеличилось в два раза. Работа, затраченная на сжатие, А = – 432 кДж. Определите: 1) какой это газ 2) чему равен первоначальный объем газа.
63. Азот массой m = 50 г находится при температуре T1 = 280 К. В результате изохорного охлаждения его давление уменьшилось в n = 2 раза, а затем в результате изобарного расширения температура газа в конечном состоянии стала равной первоначальной. Определите: 1) работу, совершенную газом; 2) изменение внутренней энергии газа.
64. Работа расширения некоторого двухатомного идеального газа составляет А = 2 кДж. Найти количество подведенной к газу теплоты, если процесс протекал а) изотермически; б) изобарно.
65. При адиабатном расширении кислорода (ν = 2 моль), находящегося при нормальных условиях, его объем увеличился в n = 3 раза. Определите: 1) изменение внутренней энергии газа; 2) работу расширения газа.
66. Азот массой m = 1 кг занимает при температуре T1 = 300 К объем V1= 0,5 м3. В результате адиабатного сжатия давление газа увеличилось в 3 раза. Определите: 1) конечный объем газа; 2) его конечную температуру; 3) изменение внутренней энергии газа.
Источник
Задача 28.
При 17°С некоторое количество газа занимает объем 580 мл. Какой объем займет это же количество газа при 100°С, если давление его останется неизменным?
Решение:
По закону Гей – Люссака при постоянном давлении объём газа изменяется прямо пропорционально абсолютной температуре (Т):
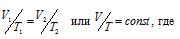
V2 – искомый объём газа;
T2 – соответствующая V2 температура;
V1 – начальный объём газа при соответствующей температуре Т1.
По условию задачи V1 = 580мл; Т1 = 290К (273 + 17 = 290) и Т2 = 373К (273 + 100 = 373). Подставляя эти значения в выражение закона Гей – Люссака, получим:
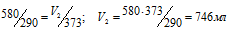
Ответ: V2 = 746мл.
Задача 29.
Давление газа, занимающего объем 2,5л, равно 121,6 кПа (912мм рт. ст.). Чему будет равно давление, если, не изменяя температуры, сжать газ до объема в 1л?
Решение:
Согласно закону Бойля – Мариотта, при постоянной температуре давление, производимое данной массой газа, обратно пропорционально объёму газа:

Обозначив искомое давление газа через Р2, можно записать:
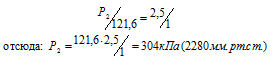
Ответ: Р2 = 304кПа (2280мм.рт.ст.).
Задача 30. На сколько градусов надо нагреть газ, находящийся в закрытом сосуде при 0 °С, чтобы давление его увеличилось вдвое?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально температуре:

По условию задачи Т1 = 0 °С + 273 = 273К; давление возросло в два раза: Р2 = 2Р1.
Подставляя эти значения в уравнение, находим:
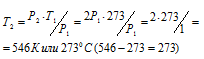
Ответ: Газ нужно нагреть на 2730С.
Задача 31.
При 27°С и давлении 720 мм.рт. ст. объем газа равен 5л. Кой объем займет это же количество газа при 39°С и давлении 104кПа?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 5л; Т = 298К (273 + 25 = 298); Р = 720 мм.рт.ст. (5,99 кПа); Р0 = 104 кПа; Т = 312К (273 + 39 = 312); Т = 273К. Подставляя данные задачи в уравнение, получим:
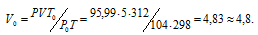
Ответ: V0 = 4,8л
Задача 32.
При 7°С давление газа в закрытом сосуде равно 96,0 кПа. Каким станет давление, если охладить сосуд до —33 °С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:

Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 96,0 кПа; Т1 = 280К (273 + 7 = 280); Т2 = 240К (273 – 33 = 240). Подставляя эти значения в уравнение, получим:
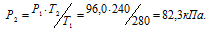
Ответ: Р2 = 82,3кПа.
Задача 33.
При нормальных условиях 1г воздуха занимает объем 773 мл. Какой объем займет та же масса воздуха при 0 °С и )и давлении, равном 93,3 кПа (700мм. рт. ст.)?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V0 = 773мл; Т0 = 298К (273 + 25 = 298); Т = 273К; Р = 93,3кПа. Подставляя данные задачи и преобразуя уравнение, получим:
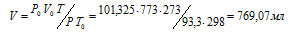
Ответ: V = 769, 07 мл.
Задача 34.
Давление газа в закрытом сосуде при 12°С равно 100 кПа (750мм рт. ст.). Каким станет давление газа, если нагреть сосуд до 30°С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:

Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 100 кПа; Т1 = 285К (273 + 12 = 285); Т2 = 303К (273 + 30 = 303). Подставляя эти значения в уравнение, получим:
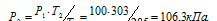
Ответ: Р2 = 106,3кПа.
Задача 35.
В стальном баллоне вместимостью 12л находится при 0°С кислород под давлением 15,2 МПа. Какой объем кислорода, находящегося при нормальных условиях можно получить из такого баллона?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 12л; Т = 273К (273 + 0 = 2273); Р =15,2МПа); Р0 = 101,325кПа; Т0 = 298К (273 + 25 = 298). Подставляя данные задачи в уравнение, получим:
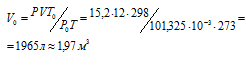
Ответ: V0 = 1,97м3.
Задача 36.
Температура азота, находящегося в стальном баллоне под давлением 12,5 МПа, равна 17°С. Предельное давление для баллона 20,3МПа. При какой температуре давление азота достигнет предельного значения?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:

Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 12,5МПа; Т1 = 290К (273 + 17 = 290); Р2 = 20,3МПа. Подставляя эти значения в уравнение, получим:
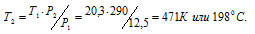
Ответ: Т2 = 1980С.
Задача 37.
При давлении 98,7кПа и температуре 91°С некоторое количество газа занимает объем 680 мл. Найти объем газа при нормальных условиях.
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:

где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V = 680мл; Т0 = 298К (273 + 25 = 298); Т = 364К (273 + 91 = 364); Р = 98,7кПа. Подставляя данные задачи и преобразуя уравнение, получим:
<
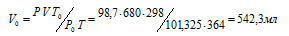
Ответ: V0 = 542,3мл.
Задача 38.
При взаимодействии 1,28г металла с водой выделилось 380 мл водорода, измеренного при 21°С и давлении 104,5кПа (784мм рт. ст.). Найти эквивалентную массу металла.
Решение:
Находим объём выделившегося водорода при нормальных условиях, используя уравнение:

где Р и V – давление и объём газа при температуре Т = 294К (273 +21 = 294); Р0 = 101,325кПа; Т0 = 273К; Р = 104,5кПа. Подставляя данные задачи в уравнение,
получим:
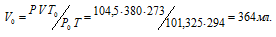
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
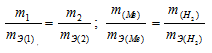
Мольный объём любого газа при н.у. равен 22,4л. Отсюда эквивалентный объём водорода равен 22,4 : 2 = 11,2л или 11200 мл. Тогда, используя формулу закона эквивалентов, рассчитаем эквивалентную массу металла:
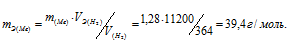
Ответ: mЭ(Ме) = 39,4г/моль.
Задача 39.
Как следует изменить условия, чтобы увеличение массы данного газа не привело к возрастанию его объема: а) понизить температуру; б) увеличить давление; в) нельзя подобрать условий?
Решение:
Для характеристики газа количеством вещества (n, моль) применяется уравнение РV = nRT, или – это уравнение Клапейрона-Менделеева. Оно связывает массу (m, кг); температуру (Т, К); давление (Р, Па) и объём (V, м3) газа с молярной массой (М, кг/моль).
Тогда из уравнения Клапейрона-Менделеева объём газа можно рассчитать по выражению:
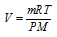
Отсюда следует, что V = const, если при увеличении массы (m) газа на некоторую величину будет соответственно уменьшена температура (T) системы на некоторое необходимое значение. Объём системы также не изменится при постоянной температуре, если при увеличении массы (m) газа на некоторую величину будет соответственно увеличено давление (P) системы на необходимую величину.
Таким образом, при увеличении массы газа объём системы не изменится, если понизить температуру системы или же увеличить давление в ней на некоторую величину.
Ответ: а); б).
Задача 40.
Какие значения температуры и давления соответствуют нормальным условиям для газов: а) t = 25 °С, Р = 760 мм. рт. ст.; б) t = 0 °С, Р = 1,013 • 105Па; в) t = 0°С, Р = 760 мм. рт. ст.?
Решение:
Состояние газа характеризуется температурой, давлением и объёмом. Если температура газа равна 0 °С (273К), а давление составляет 101325 Па (1,013 • 105) или 760 мм. рт. ст., то условия, при которых находится газ, принято считать нормальными.
Ответ: б); в).
Источник

Ответ
Ответ дан
Аккаунт удален
из уравнения состояния P*V = m*R*T/М
P1= m1*R*T/V*M1 P2 = m2*R*T/V*M2
по закону Дальтона P = P1 +P2
P= R*T * ( m1/M1 + m2/M2)/V
осталось вычислить уж сами пожалуйста работа не для клавиш