В закрытом сосуде находится 20г азота и 32 г кислорода
- Главная
- Вопросы & Ответы
- Вопрос 6478412
Суррикат Мими
более месяца назад
Просмотров : 12
Ответов : 1
Лучший ответ:
Васян Коваль
comment
более месяца назад
Ваш ответ:
Комментарий должен быть минимум 20 символов
Чтобы получить баллы за ответ войди на сайт

Лучшее из галереи за : неделю месяц все время































Другие вопросы:
Пармезан Черница
Белочке до берёзы нужно сделать 18 прыжков, а до мухомора — в 2 раза меньше. Сколько прыжков нужно сделать белочке до мухомора? Белочке до берёзы нужно сделать 18 прыжков, а до мухомора — в 2 раза &nb…
более месяца назад
Смотреть ответ
Просмотров : 17
Ответов : 1
Энджелл
На катке катались 5 девочек, а мальчиков — в 2 раза больше. Сколько на катке было мальчиков и девочек вместе? На катке катались 5 девочек, а мальчиков — в 2 раза больше. Сколько на катке было мальчико…
более месяца назад
Смотреть ответ
Просмотров : 16
Ответов : 1
Таня Масян
На одной строке обведи 4 клеточки, а на другой — в 2 раза больше. Сколько клеточек нужно обвести на второй строке? На одной строке обведи 4 клеточки, а на другой — в 2 раза больше. Сколько клеточек нужно обвести на …
более месяца назад
Смотреть ответ
Просмотров : 15
Ответов : 1
Зачетный Опарыш
Белочке до ёлки нужно сделать 6 прыжков, а до берёзы — в 3 раза больше. Сколько прыжков надо сделать белочке до берёзы? Белочке до ёлки нужно сделать 6 прыжков, а до берёзы — в 3 раза больше. Сколько прыжков надо сделать белочке до берёзы?
более месяца назад
Смотреть ответ
Просмотров : 10
Ответов : 1
Суррикат Мими
Хулиган Вася живёт в двадцатиэтажном доме. После того как Вася однажды покатался в лифте, в нём стали работать только две кнопки: «5» (при нажатии на эту Хулиган Вася живёт в двадцатиэтажном доме. После того как Вася однажды покатался в лифте, в нём стали работать только две кнопки: «5» (при нажатии…
более месяца назад
Смотреть ответ
Просмотров : 13
Ответов : 1
Источник
Решение задач – занятие, которое любит далеко не каждый. Здесь мы стараемся сделать так, чтобы оно занимало у вас поменьше времени без ущерба для качества самого решения. Тема этой статьи — задачи на внутреннюю энергию.
Подписывайтесь на наш телеграм и читайте полезные материалы для студентов каждый день!
Решение задач: внутренняя энергия
Прежде чем приступать к задачам на внутреннюю энергию тела, посмотрите общую памятку по решению физических задач. И пусть под рукой на всякий случай всегда будут основные физические формулы.
Задача №1. Изменение внутренней энергии
Условие
Воздушный шар объёмом 500 м3 наполнен гелием под давлением 105 Па. В результате нагрева температура газа в аэростате поднялась от 10 °С до 25 °С. Как увеличилась внутренняя энергия газа?
Решение
Для решения будем использовать формулу внутренней энергии идеального газа:
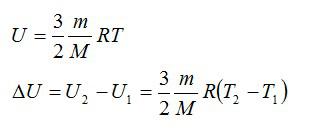
Массу гелия выразим из уравнения Клапейрона-Менделеева:
Тогда можно записать:
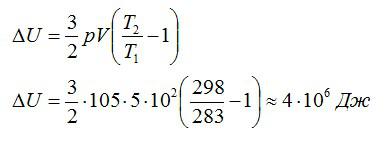
Ответ: 4 МДж.
Задача №2. Внутренняя энергия и работа
Условие
Азот массой 200 г расширяется изотермически при температуре 280 К, причем объём газа увеличивается в 2 раза. Найти:
- Изменение ∆U внутренней энергии газа.
- Совершенную при расширении газа работу А.
- Количество теплоты Q, полученное газом.
Решение
Так как процесс изотермический, то изменение внутренней энергии равно нулю, а работа равна количеству теплоты, полученному газом:
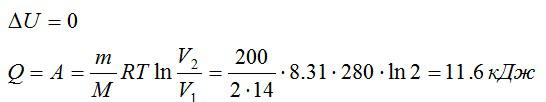
Ответ: 0; 11,6 кДж; 11,6 кДж.
Задача №3. Изменение внутренней энергии при изобарном и изохорном процессе
Условие
Кислород занимает объём V1= 3 л при давлении p1= 820 кПа. В результате изохорного нагревания и изобарного расширения газ переведён в состояние с объёмом V2= 4,5 л и давлением p2= 600 кПа. Найти количество теплоты, полученное газом; изменение внутренней энергии газа.
Решение
Теплота, подведенная к газу, идет на совершение работы и изменение внутренней энергии:
В изохорном и изобарном процессе соответственно:
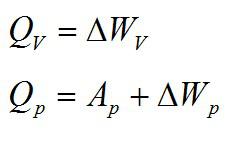
Изохорное нагревание:
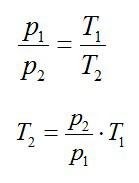
Изменение внутренней энергии при изохорном процессе:
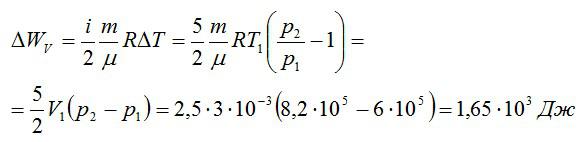
Изменение внутренней энергии при изобарном процессе:
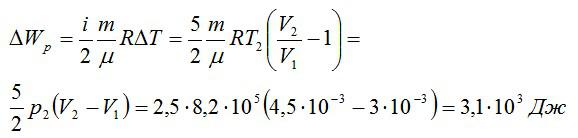
Общее изменение внутренней энергии:
Ответ: 4,75 кДж.
Задача №4. Изменение внутренней энергии двухатомного газа
Условие
Кислород массой 2 кг занимает объём 6 м3 и находится под давлением 1 атм. Газ был нагрет сначала при постоянном давлении до объёма 13 м3, а затем при постоянном объёме – до давления 23 атм. Найти изменение внутренней энергии газа.
Решение
Изменение внутренней энергии находим по формуле:
Эту форму можно преобразовать, используя уравнение Клапейрона-Менделеева:
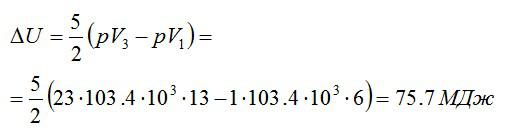
Ответ: 75,7 МДж.
Задача №5. Внутренняя энергия смеси газов
Условие
В закрытом сосуде находится масса m1 = 20 г азота и масса m2 = 32 г кислорода. Определить изменение ΔU внутренней энергии смеси газов при охлаждении ее на ΔТ = 28 К.
Решение
Определим количество молей азота и кислорода, а затем общее количество вещества в смеси соответственно:
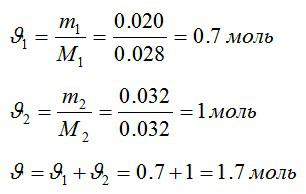
Изменение внутренней энергии:
Знак «минус» означает, что внутренняя энергия уменьшается.
Ответ: -539 Дж.
Вопросы на тему «Внутренняя энергия тела»
Вопрос 1. Что такое внутренняя энергия?
Ответ. Для начала, внутренняя энергия чего? Бутылки с пивом, воздуха в шарике, тазика с водой? Все макроскопические тела обладают энергией, заключенной внутри них: атомы твердого тела колеблются в кристаллической решетке около положений равновесия, молекулы газа находятся в постоянном хаотическом движении и т.д.
По определению:
Внутренняя энергия вещества – это энергия, которая складывается из кинетической энергии всех атомов и молекул, и потенциальной энергии их взаимодействия друг с другом.
Для идеального газа с числом степеней свободы i внутренняя энергия вычисляется по формуле:
Вопрос 2. От чего зависит внутренняя энергия идеального газа?
Ответ. Эта величина не зависит от объёма и определяется только температурой.
Вопрос 3. Как изменяется внутренняя энергия тела?
Ответ. Если тело совершает работу, его внутренняя энергия уменьшается. Например, газ передвигает поршень. Если же работа совершается над телом, то внутренняя энергия увеличивается.
Вопрос 4. Что такое функция состояния?
Ответ. Функция состояния – это один из параметров, которым можно описать термодинамическую систему. Функция состояния не зависит от того, как система пришла в то или иное состояние, а определяется несколькими переменными состояния.
Внутренняя энергия – это функция состояния термодинамической системы. В общем случае она зависит от температуры и объёма.
Вопрос 5. Можно ли изменить внутреннюю энергию тела, не совершая над ним работы?
Ответ. Да, еще один способ изменения внутренней энергии – теплопередача. В процессе теплопередачи внутренняя энергия тел изменяется.
Нужна помощь в решении задач по любой теме и других студенческих заданий? Профессиональный студенческий сервис поспособствует в выполнении работы вне зависимости от ее сложности.
Источник
Страница 1 из 2
46. Азот массой m = 10 г находится при температуре Т = 290 К. Определите: 1) среднюю кинетическую энергия одной молекулы азота; 2) среднюю кинетическую энергию вращательного движения всех молекул азота. Газ считайте идеальным.
47. Кислород массой m = 1 кг находится при температуре Т = 320 К. Определите: 1) кинетическую энергию вращательного движения молекул кислорода; 2) внутреннюю энергию молекул кислорода. Газ считайте идеальным.
48. В закрытом сосуде находится смесь азота массой m1= 56 г и кислорода массой m2 = 64 г. Определите изменение внутренней энергии этой смеси, если ее охладили на 20 °С.
49. Считая азот идеальным газом, определите его удельную теплоемкость: 1) для изохорного процесса; 2) для изобарного процесса.
50. Определите удельные теплоемкости сv и ср, если известно, что некоторый газ при нормальных условиях имеет удельный объем v = 0,7 м3/кг. Какой это газ?
51. Определите удельные теплоемкости сv и ср смеси углекислого газа массой m1 = 3 г и азота массой m2 = 4 г.
52. Определите показатель адиабаты γ для смеси газов, содержащей гелий массой m1 = 8 г и водород массой m2 = 2 г.
53. Применяя первое начало термодинамики и уравнение состояния идеального газа, покажите, что разность удельных теплоемкостей c = cp – cv = R/M.
54. Кислород массой 32 г находится в закрытом сосуде под давлением 0,1 МПа при температуре 290 К. После нагревания давление в сосуде повысилось в 4 раза. Определите: 1) объем сосуда; 2) температуру, до которой газ нагрели; 3) количество теплоты, сообщенное газом.
55. Определите количество теплоты, сообщенное газу, если в процессе изохорного нагревания кислорода объемом V = 20 л его давление изменилось на Δp = 100 кПа.
56. Двухатомный идеальный газ (ν = 2 моль) нагревают при постоянном объеме до температуры 289 К. Определите количество теплоты, которое необходимо сообщить газу, чтобы увеличить его давление в n= 3 раза.
57. При изобарном нагревании некоторого идеального газа (ν = 2 моль) на ΔT = 90 К ему было сообщено количество теплоты 5,25 кДж. Определите: 1) работу, совершаемую газом; 2) изменение внутренней энергии газа; 3) величину γ = cp/cV .
58. Азот массой m = 280 г расширяется в результате изобарного процесса при давлении p = 1 МПа. Определите: 1) работу расширения 2) конечный объем газа, если на расширение затрачена теплота Q = 5 кДж, а начальная температура азота T1 = 290 К.
59. Кислород объемом 1 л находится под давлением 1 МПа. Определите, какое количество теплоты необходимо сообщить газу, чтобы: 1) увеличить его объем вдвое в результате изобарного процесса; 2) увеличить его давление вдвое в результате изохорного процесса.
60. Некоторый газ массой m = 5 г расширяется изотермически от объема V1до объема V2 = 2V1. Работа расширения A= 1 кДж. Определите среднюю квадратичную скорость молекул газа.
61. Азот массой m = 14 г сжимают изотермически при температуре T = 300 К от давления p1 = 100 кПа до давления p2= 500 кПа. Определите: 1) изменение внутренней энергии газа; 2) работу сжатия; 3) количество выделившейся теплоты.
62. Некоторый газ массой 1 кг находится при температуре Т = 300 К и под давлением p1 = 0.5 МПа. В результате изотермического сжатия давление газа увеличилось в два раза. Работа, затраченная на сжатие, А = – 432 кДж. Определите: 1) какой это газ 2) чему равен первоначальный объем газа.
63. Азот массой m = 50 г находится при температуре T1 = 280 К. В результате изохорного охлаждения его давление уменьшилось в n = 2 раза, а затем в результате изобарного расширения температура газа в конечном состоянии стала равной первоначальной. Определите: 1) работу, совершенную газом; 2) изменение внутренней энергии газа.
64. Работа расширения некоторого двухатомного идеального газа составляет А = 2 кДж. Найти количество подведенной к газу теплоты, если процесс протекал а) изотермически; б) изобарно.
65. При адиабатном расширении кислорода (ν = 2 моль), находящегося при нормальных условиях, его объем увеличился в n = 3 раза. Определите: 1) изменение внутренней энергии газа; 2) работу расширения газа.
66. Азот массой m = 1 кг занимает при температуре T1 = 300 К объем V1= 0,5 м3. В результате адиабатного сжатия давление газа увеличилось в 3 раза. Определите: 1) конечный объем газа; 2) его конечную температуру; 3) изменение внутренней энергии газа.
Источник
В
условиях задач этого раздела температура задается в градусах Цельсия.
При проведении числовых расчетов необходимо перевести температуру в
градусы Кельвина, исходя из того, что 0° С = 273° К. Кроме того,
необходимо также представить все остальные величины в единицах системы
СИ. Так, например, 1л = 10-3 м3; 1м3 = 106 см3 = 109 мм3.Если
в задаче приведена графическая зависимость нескольких величин от
какой-либо одной и при этом все кривые изображены на одном графике, то
по оси у задаются условные единицы. При решении задач используются данные таблиц 3,6 и таблиц 9—11 из приложения.
5.1. Какую температуру T имеет масса m = 2 г азота, занимающего объем V = 820 см3 при давлении p = 0,2 МПа?
5.2. Какой объем V занимает масса m = 10г кислорода при давлении р = 100 кПа и температуре t = 20° С?
5.3. Баллон объемом V = 12 л наполнен азотом при давлении p = 8,1МПа и температуре t = 17° С. Какая масса m азота находится в баллоне?
5.4. Давление воздуха внутри плотно закупоренной бутылки при температуре t1=7C было p1= 100 кПа. При нагревании бутылки пробка вылетела. До какой температуры t2нагрели бутылку, если известно, что пробка вылетела при давлении воздуха в бутылке p = 130 кПа?
5.5. Каким должен быть наименьшей объем V баллона, вмещающего массу m = 6,4 кг кислорода, если его стенки при температуре t = 20° С выдерживают давление p = 15,7 МПа?
5.7. Найти массу m сернистого газа (S02), занимающего
объем V = 25 л при температуре t=27С и давлении p = 100 кПа.
5.6. В баллоне находилась масса m1= 10 кг газа при давлении p1 = 10 МПа. Какую массу Am газа взяли из баллона, если давление стало равным p2= 2,5 МПа? Температуру газа считать постоянной.
5.8. Найти массу m воздуха, заполняющего аудиторию высотой h = 5 м и площадью пола S = 200 м2. Давление воздуха p = 100кПа, температура помещения t = 17° С. Молярная масса воздуха u = 0,029 кг/моль.
5.9. Во сколько раз плотность воздуха p1, заполняющего помещение зимой (t1 =7°С), больше его плотности p2летом (t2=37° С)? Давление газа считать постоянным.
5.10. Начертить изотермы массы m = 0,5 г водорода для температур: а) t1 = 0° С; б) t2 = 100° С.
5.11. Начертить изотермы массы m = 15,5г кислорода для температур: a) t1 = 39° С; б) t2 =180° С.
5.12. Какое количество v газа находится в баллоне объемом V = 10 м3 при давлении p =96 кПа и температуре t = 17° С?
5.13. Массу m =5 г азота, находящегося, в закрытом сосуде объемом V = 4 л при температуре t1 = 20° С, нагревают до температуры t2 = 40° С. Найти давление p1 и p2газа до и после нагревания.
5.14. Посередине откачанного и запаянного с обеих концов капилляра,
расположенного горизонтально, находится столбик ртути длиной l = 20 см.
Если капилляр поставить вертикально, то столбик ртути переместится на dl
= 10 см. До какого давления p0был откачан капилляр? Длина капилляра L –1 м.
5.15. Общеизвестен шуточный вопрос: «Что тяжелее: тонна свинца или
тонна пробки?» На сколько истинный вес пробки, которая в воздухе весит
9,8кН, больше истинного веса свинца, который в воздухе весит также
9,8кН? Температура воздуха t = 17° С, давление p = 100кПа.
5.16. Каков должен быть вес p оболочки детского воздушного шарика, наполненного водородом, чтобы результирующая подъемная сила шарика F =
0 , т.е. чтобы шарик находился во взвешенном состоянии? Воздух и
водород находится при нормальных условиях. Давление внутри шарика равно
внешнему давлению. Радиус шарика r = 12,5 см.
5.17. При температуре t = 50° С давление насыщенного водяного пара p = 12,3 кПа. Найти плотность p водяного пара.
5.18. Найти плотность p водорода при температуре t = 10° С и давлении p = 97,3 кПа.
5.19. Некоторый газ при температуре t = 10° С и давлении p = 200 кПа имеет плотность p = 0,34 кг/м3. Найти молярную массу u газа.
5.20. Сосуд откачан до давления p = 1,33 • 10-9 Па; температура воздуха t = 15° С. Найти плотность p воздуха в сосуде.
5.21. Масса m = 12 г газа занимает объем V = 4 л при температуре t1 = 7° С. После нагревания газа при постоянном давлении его плотность стала равной p = 0,6 кг/м3. До какой температуры г, нагрели газ?
5.22. Масса m = 10г кислорода находится при давлении p = 304 кПа и температуре t1=10° С. После расширения вследствие нагревания при постоянном давлении кислород занял объ-
ем V2=10 л. Найти объем V1газа до расширения, температуру t2 газа после расширения, плотности p1и p2газа до и после расширения.
5.23. В запаянном сосуде находится вода, занимающая объем, равный половине объема сосуда. Найти давление p и плотность
p водяного пара при температуре t = 400° С, зная, что при этой
температуре вся вода обращается в пар.
5,24. Построить график зависимости плотности p кислорода: а) от давления p при температуре Т = const = 390 К в интервале
0 < p < 400 кПа через каждые 50 кПа; б) от температуры Т при p = const = 400 кПа в интервале 200 < Т < 300 К через каждые 20К.
5.25. В закрытом сосуде объемом V = 1 м3 находится масса m1= 1,6 кг кислорода и масса m2= 0,9 кг воды. Найти давление p в сосуде при температуре t = 500° С, зная, что при этой температуре вся вода превращается в пар.
5.26. В сосуде 1 объем V1 = 3 л находится газ под давлением p1= 0,2 МПа. В сосуде 2 объем V2 = 4 л находится тот же газ под давлением p2= 0,1 МПа. Температуры газа в обоих сосудах одинаковы. Под каким давлением p будет находиться газ, если соединить сосуды 1 и 2 трубкой?
5.27. В сосуде объемом V = 2 л находится масса m1= 6 г углекислого газа (С02) и масса m2закиси азота (N20) при температуре t = 127° С. Найти давление p смеси в сосуде.
5.28. В сосуде находится масса m1 = 14 г азота и масса m2=9гводорода при температуре t = 10°С и давлении p = 1 МПа. Найти молярную массу p смеси и объем V сосуда.
5.29. Закрытый сосуд объемом V = 2 л наполнен воздухом при нормальных условиях. В сосуд вводится диэтиловый эфир (С2Н5ОС2Ы5). После того как весь эфир испарился, давление в сосуде стало равным p = 0,14 МПа. Какая масса m эфира была введена в сосуд?
5.30. В сосуде объемом V = 0,5 л находится масса m = 1 г парообразного йода (I2). При температуре t = 1000° С давление в сосуде pс= 93,3 кПа. Найти степень диссоциации а молекул йода на атомы. Молярная масса молекул йода u = 0,254 кг/моль.
5.31. В сосуде находится углекислый газ. При некоторой температуре
степень диссоциации молекул углекислого газа на кислород и окись
углерода а = 0,25 . Во сколько раз давление в сосуде при этих
условиях будет больше того давления, которое имело бы место, если бы
молекулы углекислого газа не были диссоциированы?
5.32. В воздухе содержится 23,6% кислорода и 76,4% азота (по массе) при давлении p = 100кПа и температуре t = 13° С.
Найти плотность p воздуха и парциальные давления p1и p2
кислорода и азота.
5.33. В сосуде находится масса m1 = 10 г углекислого газа и масса m2=15г азота. Найти плотность p смеси при температуре t = 27° С и давлении p = 150 кПа.
5.34. Найти массу m0атома: а) водорода; б) гелия.
5.35. Молекула азота, летящая со скоростью v = 600 м/с, упруго ударяется о стенку сосуда по нормали к ней. Найти импульс силы Fdt, полученный стенкой сосуда за время удара.
5.36, Молекула аргона, летящая со скоростью v = 500 м/с, упруго
ударяется о стенку сосуда. Направление скорости молекулы и нормаль к
стенке сосуда составляют угол а = 60° . Найти импульс силы Fdt, полученный стенкой сосуда за время удара.
5.37. Молекула азота летит со скоростью v = 430 м/с. Найти импульс mv этой молекулы.
5.38. Какое число молекул n содержит единица массы водяного пара?
5.39. В сосуде объемом V = 4 л находится масса m = 1 г водорода. Какое число молекул n содержит единица объема сосуда?
5.40. Какое число молекул N находится в комнате объемом V = 80 m3 при температуре t = 17° С и давлении p = 100 кПа?
5.41. Какое число молекул и содержит единица объема сосуда при температуре t = 10° С и давлении p = 1,33 * 10-9 Па?
5.42. Для получения хорошего вакуума в стеклянном сосуде необходимо
подогревать стенки сосуда при откачке для удаления адсорбированного
газа. На сколько может повыситься давление в сферическом сосуде радиусом
r = 10 см, если адсорбированные молекулы перейдут со стенок в сосуд? Площадь поперечного сечения молекул s0= 10-19 м2. Температура газа в сосуде t = 300° С. Слой молекул на стенках считать мономолекулярным.
5.43. Какое число частиц находится в единице массы парообразного йода (I2), степень диссоциации которого а = 0,5 ? Молярная масса молекулярного йода u = 0,254 кг/моль.
5.44. Какое число частиц N находится в массе m = 16г кислорода, степень диссоциации которого а = 0,5 ?
5.45. В сосуде находится количество v1=10-7 молей кислорода и масса m2=10-6г азота. Температура смеси t = 100° С, давление в сосуде p = 133мПа. Найти объем V сосуда, парциальные давления p1и p2кислорода и азота и число молекул n в единице объема сосуда.
5.46. Найти среднюю квадратичную скорость молекул воздуха при температуре t = 17° С. Молярная масса воздуха u = 0,029 кг/моль.
5.48. В момент взрыва атомной бомбы развивается температура T=107 К.
Считая, что при такой температуре все молекулы полностью диссоциированы
на атомы, а атомы ионизированы, найти среднюю квадратичную скорость
sqr(v2) иона водорода.
5.47. Найти отношение средних квадратичных скоростей молекул гелия и азота при одинаковых температурах.
5.49. Найти число молекул nводорода в единице объема сосуда при давлении p = 266,6 Па, если средняя квадратичная
скорость его молекул sqr(v2)= 2,4 км/с.
5.50. Плотность некоторого газа p = 0,06 кг, средняя
квадратичная скорость его молекул sqr(v2) = 500 м/с. Найти
давление p, которое газ оказывает на стенки сосуда.
5.51. Во сколько раз средняя квадратичная скорость пылинки, взвешенной в воздухе, меньше средней квадратичной скорости
молекул воздуха? Масса пылинки /77 = 10~8г. Воздух считать однородным газом, молярная масса которого // = 0,029 кг/моль.
5.52. Найти импульс mv молекулы водорода при температуре t = 20° С. Скорость молекулы считать равной средней квадратичной скорости.
5.53. В сосуде объемом V = 2лнаходится масса m = 10 г кислорода при давлении p = 90,6 кПа. Найти среднюю
5.216. Найти изменение dS энтропии при превращении массы m = 10 г льда (t = -20° С) в пар (tn = 100° С).
5.55. Средняя квадратичная скорость молекул некоторого
газа sqr(v2) = 450 м/с. Давление газа p = 50 кПа. Найти плотность p газа при этих условиях.
5.56. Плотность некоторого газа p = 0,082 кг/м3 при давлении p = 100кПа и температуре t = 17° С. Найти среднюю квадратичную скорость sqr(v2) молекул газа. Какова молярная масса p этого газа?
5.218. Найти изменение dS энтропии при плавлении массы m = 1кг льда (t = 0° С).
5.219. Массу m = 640 г расплавленного свинца при температуре плавления tплвылили на лед (t = 0° С). Найти изменение dS энтропии при этом процессе.
5.60. Найти энергию Wврвращательного движения молекул, содержащихся в массе m = 1 кг азота при температуре t = 7° С.
5.61. Найти внутреннюю энергию W двухатомного газа, находящегося в сосуде объемом V = 2л под давлением p = 150 кПа.
5.62. Энергия поступательного движения молекул азота, находящегося в баллоне объем V = 20 л, W = 5 кДж, а средняя квадратичная скорость его молекул sqr(v2) = 2*103 м/с. Найти массу m азота в баллоне и давление /?, под которым он находится.
5.63. При какой температуре Т энергия теплового
движения атомов гелия будет достаточна для того, чтобы атомы гелия
преодолели земное тяготние и навсегда покинули земную атмосферу? Решить
аналогичную задачу для Луны.
5.64. Масса m = 1 кг двухатомного газа находится под давлением p = 80кПа и имеет плотность p = 4кг/м3. Найти
энергию теплового движения W молекул газа при этих условиях.
5.65. Какое число молекул N двухатомного газа содержит объем V = 10см3 при давлении V = 5,3 кПа и температуре
t = 27° С? Какой энергией теплового движения W обладают эти молекулы?
5.66. Найти удельную теплоемкость cкислорода для: а) V = const; б) p = const.
5.67. Найти удельную теплоемкость сp: а) хлористого водорода; б) неона; в) окиси азота; г) окиси углерода; д) паров ртути.
5.68. Найти отношение удельных теплоемкостей сp/сtдля кислорода.
5.69. Удельная теплоемкость некоторого двухатомного газа с = 14,7 кДж/(кг-К). Найти молярную массу u этого газа.
5.70. Плотность некоторого двухатомного газа при нормальных условиях p = 1,43 кг/м3. Найти удельные теплоемкости сt и
сpэтого газа.
5.71. Молярная масса некоторого газа u = 0,03 кг/моль, отношение сp/сV = 1,4 . Найти удельные теплоемкости сV и сpэтого газа.
5.72. Во сколько раз молярная теплоемкость С гремучего газа больше молярной теплоемкости С” водяного пара, получившегося при его сгорании? Задачу решить для: а) V = const б) p = const.
5.73. Найти степень диссоциации а кислорода, если его удельная теплоемкость при постоянном давлении ср= 1,05 кДж/(кг-К).
5.74. Найти удельные теплоемкости сV и сp парообразного йода (I2), если степень диссоциации его а = 0,5. Молярная масса молекулярного йода u = 0,254 кг/моль.
5.75. Найти степень диссоциация а азота, если для него отношение сp /сV = 1,47.
5.76. Найти удельную теплоемкость сpгазовой смеси, состоящей из количества v1=Зкмоль аргона и количества v2 = 3 кмоль азота.
5.77. Найти отношение сp/сV для газовой смеси, состоящей из массы m1 = 8 г гелия и массы m2 = 16 г кислорода.
5.78. Удельная теплоемкость газовой смеси, состоящей из количества v1= 1 кмоль кислорода и некоторой массы m2аргона
равна сV = 430 Дж/(кгК),. Какая масса m2аргона находится в газовой смеси?
5.79. Масса m = 10 г кислорода находится при давлении p = 0,3 МПа и температуре t = 10° С. После нагревания при
p= const газ занял объем V2 =10л. Найти количество теплоты
Q, полученное газом, и энергию теплового движения молекул
газа W до и после нагревания.
5.80. Масса m = 12 г азота находится в закрытом сосуде объемом V =2л при температуре t = 10° С. После нагревания Давление в сосуде стало равным p = 1,33 МПа. Какое количество теплоты Q сообщено газу при нагревании?
Источник
