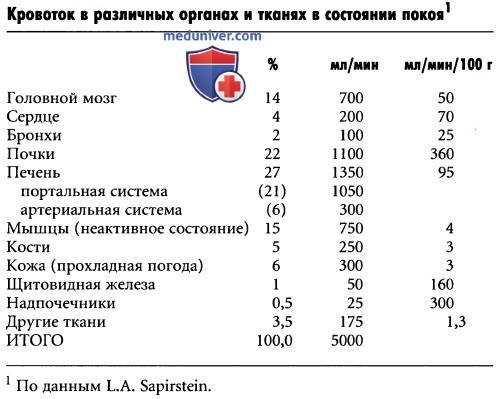
Васкуляция сосудов возрастные изменения

Васкуляризация и иннервация сосудов. В средней и наружной оболочках крупных и средних сосудов проходят питающие сосуды (vasa vasorum) и нервные стволики (nervi vasorum). Питание внутренней оболочки осуществляется диффузно из крови, протекающей по сосуду. В венах сосуды сосудов проникают и во внутреннюю оболочку, чему благоприятствует низкое давление в сосуде.
Сосуды иннервируются вегетативной нервной системой. Нервы, содержащие миелиновые и безмиелиновые нервные волокна, образуют интра- и периваскулярные адренергические нервные сплетения. Чувствительные нервные окончания содержаться во всех оболочках сосуда (афферентная иннервация осуществляется псевдоуниполярными нейронами спинальных ганглиев). Двигательные окончания — находятся на гладких миоцитах.
Эффект вазоконстрикции реализуется посредством сосудосуживающих симпатических нервных волокон через µ- и b-адренорецепторы, а также гуморально эндотелином-1, продуцируемым эндотелием.
Вазодилатация также осуществляется гуморальными факторами эндотелия (оксид азота, простациклин) и др.
Холинергическая парасимпатическая иннервация сосудов, приводящая к вазодилатации, характерна для сосудов наружных половых органов и мелких артерий мягкой мозговой оболочки, почек, легких, матки и др.
Особое место в нервной регуляции сосудистого тонуса играют рефлексогенные зоны, реагирующие на изменения химизма циркулирующей крови. К ним относятся пещеристое сплетение, каротидный синус, каротидный клубочек устья легочных вен и аорты. Они содержат специальные клетки к которым подходят афферентные и эфферентные нервные волокна. Возбуждение афферентных волокон вызывает выделение клетками вазодилататоров. Возбуждение по этим волокнам передается в нервные центры, изменяющие работу сердца и сосудов.
Возрастные изменения. Сосуды новорожденных характеризуются большей емкостью по отношению к массе тела, чем у взрослого; в стенке сосудов слабее выражен эластический каркас; меньше развита мышечная оболочка; диаметры соответствующих артерий и вен обычно одинаковы (у взрослого диаметр вены больше). Нет выраженных различий между типами артерий (они появляются к концу первого месяца жизни). Полное формирование сосудов завершается к 12 годам. Перестройка сосудов под влиянием нагрузки завершается к 30 годам.
При старении структура сосудистой стенки изменяется следующим образом:
1) в результате склеротических процессов внутренняя оболочка резко утолщается;
2) мышечная оболочка истончается из-за частичной атрофии гладких миоцитов;
3) эластический каркас подвергается распаду и фрагментации;
4) происходит физиологическое разрастание соединительной ткани, накопление сульфатированных гликозаминогликанов.
5) в гемокапиллярах снижается резистентность стенки, повышается их ломкость, уменьшается число эндотелиоцитов, утолщается базальная мембрана. В тканях появляются участки с запустевающими капиллярами, что ведет к снижению уровня транскапиллярного обмена.
Все эти изменения ведут к потере эластичности и нарушению адаптивных возможностей сосудистой стенки, а также к уменьшению просвета сосудов, возрастанию ригидности их стенки, способствуют атеросклерозу и кальцификации.
Регенерация. Сосудистая стенка имеет высокие резервные возможности, обладает высокой пластичностью и способностью к адаптации, регенерации компенсации. Она способна подвергаться гиперплазии либо, наоборот, редуцироваться в соответствии с изменяющимися условиями функционирования организма. Эта способность обусловлена тем, что в стенка сосудов образована камбиальными обновляющимися тканями и хорошо регенерирует.
Физиологическая регенерация протекает непрерывно во всех оболочках и слоях. Обновляется как клеточный состав, так межклеточное вещество. За счет деления мозаично расположенных камбиальных эндотелиоцитов восстанавливается эндотелий. Полноценные эндотелиоциты могут слущиваться в одном участке и, попадая в кровоток, затем прикрепляться в эндотелиальный пласт в другом месте, вступая в пролиферацию. Гладкие миоциты также имеют камбий и их количество поддерживается на постоянном уровне. Тесные взаимодействия эндотелия и гладких миоцитов, их митотическая активность регулируется за счет секретируемых медиаторов. Высокой пролиферативной способностью обладают и фибробласты адвентициальной оболочки.
Репаративная регенерация различна в разных сосудах.
В крупных магистральных сосудах участки значительных деструктивных и некротических изменений заживают рубцеванием. В последствии здесь часто формируются аневризмы — истончения и выпячивания стенки с возможностью их разрыва. Полное восстановление таких сосудов возможно лишь при небольших дефектах. При удалении отрезка сосуда регенерация может наступить только с помощью протеза.
Мелкие сосуды, особенно сосуды микроциркуляторного русла, регенерируют после травмы очень хорошо. Уже к концу первых соток после повреждения в стенке сосуда начинается деление эндотелиальных клеток. Образуется эндотелиальная почка. Затем в ней либо образуются вакуоли, которые потом сливаются и формируют просвет сосуда; либо просвет сосуда образуется за счет межклеточных соединений эндотелиоцитов, сформировавших два ряда. Далее активизируются адвентициальные клетки и перициты. Мышечные клетки восстанавливаются более медленно.
ТЕМА 14
Источник
Возрастные изменения
Строение сосудов непрерывно меняется в течение всей жизни человека. Развитие сосудов под влиянием функциональной нагрузки заканчивается примерно к 30 годам. В дальнейшем в стенках артерий происходит разрастание соединительной ткани, что ведет к их уплотнению. В артериях эластического типа этот процесс выражен сильнее, чем в остальных артериях. После 60-70 лет во внутренней оболочке всех артерий обнаруживаются очаговые утолщения коллагеновых волокон, в результате чего в крупных артериях внутренняя оболочка по размерам приближается к средней. В мелких и средних артериях внутренняя оболочка разрастается слабее. Внутренняя эластическая мембрана с возрастом постепенно истончается и расщепляется. Мышечные клетки средней оболочки атрофируются. Эластические волокна подвергаются распаду и фрагментации, в то время как коллагеновые волокна разрастаются. Одновременно с этим во внутренней и средней оболочках у пожилых людей появляются известковые и липидные отложения, которые прогрессируют с возрастом. В наружной оболочке у лиц старше 60-70 лет возникают продольно лежащие пучки гладких мышечных клеток.
Возрастные изменения в венах сходны с таковыми в артериях. Однако перестройка стенки вены человека начинается еще на первом году жизни. – К моменту рождения человека в средней оболочке стенок бедренной и подкожных вен нижних конечностей имеются лишь пучки циркулярно ориентированных мышечных клеток. Только к моменту вставания на ноги (к концу первого года) и повышения гидростатического давления развиваются продольные мышечные пучки. У детей просвет вены примерно равен просвету соответствующей артерии, а у взрослых по просвет вены примерно вдвое больше просвета соответствующей артерии. Расширение просвета вен обусловлено меньшей эластичностью их стенки.
Сосуды сосудов до возраста 50-60 лет, как правило, бывают умеренно спазмированными, а после 60 лет просвет их расширяется.
Лимфатические сосуды многих органов у лиц старческого возраста характеризуются многочисленными мелкими варикозными вздутиями и выпячиваниями. Во внутренней оболочке стенок крупных лимфатических стволов и грудного протока у людей старше 35 лет увеличивается количество коллагеновых волокон. Одновременно количество мышечных клеток и эластических волокон уменьшается.
Регенерация
Мелкие кровеносные и лимфатические сосуды обладают способностью к регенерации. Восстановление дефектов сосудистой стенки после ее повреждения начинается с регенерации и роста ее эндотелия. Уже к концу первых – началу вторых суток на месте нанесенного повреждения наблюдается пролиферация эндотелиальных клеток.
В регенерации сосудов после травмы принимают участие эндотелиоциты, адвентициальные клетки, а в мелких сосудах – и перициты.
Мышечные клетки поврежденного сосуда, как правило, восстанавливаются более медленно и неполно по сравнению с другими тканевыми элементами сосуда. Восстановление их происходит частично путем деления миоцитов, а также в результате дифференцировки миофибробластов. Эластические элементы развиваются слабо. В случае перерыва среднего и крупного сосудов регенерации его стенки без оперативного вмешательства, как правило, не наступает, хотя восстановление циркуляции крови в соответствующей области может наблюдаться очень рано. Это происходит, с одной стороны, благодаря компенсаторной перестройке коллатеральных сосудов, а с другой – вследствие развития и роста новых мелких сосудов – капилляров.
Новообразование капилляров начинается с того, что цитоплазма эндотелиальных клеток артериол и венул набухает в виде почки, затем эндотелиальные клетки подвергаются делению. По мере роста эндотелиальной почки в ней появляется полость. Такие слепо заканчивающиеся трубки растут навстречу друг другу и смыкаются концами. Цитоплазматические перегородки между ними истончаются и прорываются, и во вновь образованном капилляре устанавливается циркуляция крови.
Лимфатические сосуды после их повреждения регенерируют несколько медленнее, чем кровеносные. Регенерация лимфатических сосудов может происходить за счет или почкования дистальных концов эндотелиальных трубок, или перестройки лимфатических капилляров в отводящие сосуды.
Источник
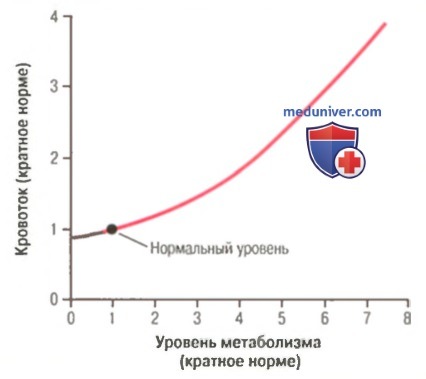
Васкуляризация тканей. Формирование и рост новых кровеносных сосудовОсновным механизмом долговременной регуляции местного кровотока является изменение количества кровеносных сосудов в тканях. Так, длительная активизация метаболических процессов в данной ткани вызывает усиленную васкуляризацию ткани; если же уровень метаболизма снижается, количество кровеносных сосудов в ткани уменьшается. Так происходит изменение васкуляризации тканей в зависимости от их метаболических потребностей. Эта реконструкция сосудистой системы развивается быстро (через несколько дней) у очень молодых животных, а также в быстрорастущих тканях зрелого организма (например, в рубцовой ткани или в растущей опухоли). И наоборот, в зрелых, высокодифференцированных тканях подобный процесс протекает медленно. Таким образом, на долговременную регуляцию кровотока требуется всего несколько дней у новорожденных, и более месяца — у лиц старшего возраста. Кроме того, результат перестройки сосудистого русла оказывается гораздо лучшим в молодых тканях. Так, у новорожденных сосудистая сеть способна практически полностью удовлетворять возросшие потребности тканей, в то время как в зрелых тканях васкуляризация зачастую намного отстает от потребностей ткани. Роль кислорода в долговременной регуляции. Кислород имеет большое значение не только в быстрой краткосрочной регуляции местного кровотока, но и в долговременной регуляции. Одним из примеров является усиленная васкуляризация тканей у животных, обитающих на больших высотах, где содержание кислорода в атмосфере низкое. Другим примером может быть наблюдение за куриными зародышами, развивающимися в условиях гипоксии, у которых число кровеносных сосудов в 2 раза превышает нормальную плотность сосудов в тканях. Подобный эффект может иметь самые неблагоприятные последствия у недоношенных детей, помещенных в кислородную палатку с лечебными целями. Избыток кислорода немедленно прекращает рост сосудов сетчатки глаза у недоношенного ребенка и даже вызывает дегенерацию уже имеющихся сосудов. Затем, когда ребенка извлекают из кислородной палатки, начинается бурный рост сосудов в тканях глазного яблока, и кровеносные сосуды прорастают в стекловидное тело глаза, что приводит к слепоте. Такое явление называют ретроленталъной фиброплазией.
Формирование и рост новых кровеносных сосудовОбнаружены более 10 факторов, которые усиливают рост новых кровеносных сосудов. Почти все они являются короткими пептидами, из них 3 фактора изучены лучше других: сосудистый эндотелиальный фактор роста, фактор роста фибробластов и ангиогенин. Каждый из них был выделен из тканей с неадекватно низким кровоснабжением. По-видимому, дефицит кислорода или питательных веществ (или и того, и другого) приводит к образованию сосудистых факторов роста (так называемых ангиогенных факторов). В сущности, все ангиогенные факторы вызывают рост новых сосудов одинаковым способом: они способствуют появлению новых сосудов путем разрастания и ветвления старых сосудов. Первым этапом этого процесса является растворение базальной мембраны эндотелия в точке ветвления. Затем начинается быстрое образование новых эндотелиальных клеток, которые мигрируют через сосудистую стенку, образуя сосудистый росток, направленный к источнику ангиогенных факторов. Клетки продолжают быстро делиться и свертываются в трубку. Трубка соединяется с другой такой же, формирующейся от другого сосуда (артериолы или венулы), — и появляется капиллярная петля, в которой начинается кровоток. Если кровоток достаточно велик, в стенку нового сосуда переселяются гладкомышечные клетки, сосуд становится артериолой или венулой, а иногда и более крупным сосудом. Так, ангиогенез объясняет механизм, с помощью которого метаболические факторы тканей способствуют росту новых сосудов. Ряд других веществ, таких как некоторые стероидные гормоны, оказывают на мелкие кровеносные сосуды противоположное действие. При этом происходит разрушение сосудистых клеток и исчезновение сосудов. Следовательно, количество кровеносных сосудов может уменьшаться, когда необходимость в них отпадает.
Васкуляризация зависит от максимальной потребности тканей в кровоснабжении, а не от среднего уровня кровоснабжения. Исключительно важной характеристикой долговременной регуляции кровоснабжения является то, что васкуляризация тканей обусловлена главным образом максимальным уровнем кровотока, необходимого тканям, а не средним уровнем их потребностей. Необходимость в таком максимальном кровотоке может возникать не более чем на несколько минут в день. Тем не менее, даже такой кратковременной предельной нагрузки достаточно для выделения эндотелиальных факторов роста в мышечной ткани, чтобы усилить ее васкуляризацию. Если этого не происходит, каждый раз, когда человеку приходится выполнять тяжелую физическую нагрузку, его мышцы не могут развить необходимую силу сокращения, т.к. они не получают достаточного количества кислорода и питательных веществ. Однако если избыточная васкуляризация произошла, большая часть кровеносных сосудов обычно пребывает в состоянии сужения. Они открываются только под действием местных факторов, таких как недостаток кислорода, влияние сосудорасширяющих нервов и других факторов, свидетельствующих о необходимости резко увеличить кровоток. – Также рекомендуем “Коллатеральное кровообращение. Гуморальная регуляция кровообращения” Оглавление темы “Регуляция кровоснабжения”: |
Источник
Содержание темы “Атеросклероз и другие формы артериосклероза.”: Возрастные изменения артерий.
С функциональной точки зрения эти возрастные изменения приводят к постепенному повышению ригидности сосудов. Крупные артерии могут расшириться, удлиниться, стать извитыми. В области циркулярных дегенеративных атеросклеротических бляшек могут сформироваться аневризмы. Такие деформирующие изменения нередко пропорциональны диаметру сосуда и коррелируют с наличием ветвей, изгибов и анатомических точек соприкосновения. Выраженность внешнего поддерживающего каркаса также определяет способность сосудов, ослабленных вследствие потери эластичности, противостоять гидростатическому давлению. Именно это обусловливает особую уязвимость сосудов мозга, лишенных окружающей поддержки. Несмотря на то что увядание сопровождается утолщением внутренней оболочки, являющимся признаком местного атероматоза, возрастные изменения и артериосклероз являются двумя различными, не связанными друг с другом процессами. Неатероматозные формы атеросклерозаАтеросклероз затрагивает прежде всего внутреннюю оболочку и чаще поражает брюшную аорту и ее крупные ветви – почечные артерии и артерии нижних конечностей, а также венечные артерии и сосуды мозга. Он может сопровождать или ускорять развитие других основных форм артериосклероза: локальную кальцификацию и артериолосклероз (табл. 195-2). Локальная (очаговая) кальцификация артерии. С атеросклерозом не следует путать очаговую кальцификацию среднего слоя (медии), поражающую главным образом артерии мышечного типа среднего диаметра. Этот тип артериосклероза получил название артериосклероза Менкеберга. Артериосклерозу Менкеберга чаще всего подвержены артерии нижних и верхних конечностей, а также половых органов как у мужчин, так и у женщин. Это заболевание редко встречается у лиц моложе 50 лет. Процесс заключается в дегенерации гладких мышечных клеток с последующим замещением их кальциевыми отложениями. Сосуды становятся твердыми, извитыми. При пальпации артерий, доступных для этого метода исследования (например, лучевой), у врача может возникнуть ощущение, что его пальцы касаются ригидного жгута. Рентгенологически подобные сосуды характеризуются наличием регулярно повторяющихся концентрических кальцификатов преимущественно в сосудистом русле таза и бедер. Изолированные изменения только срединного слоя не приводят к сужению просвета сосуда и незначительно влияют на кровообращение, вследствие чего имеют небольшое клиническое значение. Однако медиальный склероз сосудов нижних конечностей часто сочетается с атеросклерозом, приводя к окклюзии артерий. Подобные изменения преобладают у людей пожилого возраста и у лиц, длительное время получавших кортикостероиды. У больных сахарным диабетом очаговая Кальцификация протекает быстро и принимает тяжелую форму. Наиболее часто она встречается в тех случаях, когда сахарный диабет осложняется невропатией. При этом считается, что в качестве этиологического фактора выступает симпатическая денервация гладких мышц средней оболочки. Таблица 195-2. Заболевания, сочетающиеся с ранним артериосклерозом Атеросклероз Неатероматозный артериосклероз У людей пожилого возраста встречается очаговое кальцифицирующее поражение клапана аорты. С возрастом происходит постепенное накопление кальция на аортальной поверхности клапана, в результате чего появляются различные клинические симптомы, спектр которых варьирует от безобидного систолического шума до тяжелого кальцифицированного стеноза устья аорты. Артериолосклероз. В основе этого заболевания лежат образование гиалина и дегенеративные изменения как внутренней, так и средней оболочек мелких артерий и артериол, в частности селезенки, поджелудочной железы, надпочечников и почек. Артериолосклероз почек (но необязательно других органов) практически всегда сопровождается гипертензией. Более легкие случаи стойкой гипертензии характеризуются гиалинизацией почечных артериол. Более тяжелая или злокачественная гипертензия приводит к развитию типичной фиброзной и эластической гиперплазии и даже некроза внутренней и средней оболочек. -Читать далее>>>> |
Источник