Видео сосуды у новорожденных
Кровообращение новорожденного. Как течет кровь у новорожденного?
После рождения ребенка совершаются процессы адаптации к постнатальной жизни. В этот период прекращается плацентарный кровоток, функция газообмена переходит к легким, и закрываются фетальные коммуникации. Малый и большой круги кровообращения становятся последовательными. Сопротивление легочных сосудов прогрессивно снижается из-за их раскрытия, а в артериальном русле – повышается (из-за потери плаценты, обладающей низким сопротивлением).
После первого вдоха и начала легочной вентиляции резко возрастает легочный кровоток, перераспределяется сердечный выброс, меняется нагрузка на желудочки. Весь поток крови из легких теперь возвращается в левый желудочек, существенно превышая объем, попадавший в него внутриутробно; сразу после рождения левый желудочек увеличивает свой выброс в 3-6 раз больше, чем правый желудочек. Это сопровождается почти двухкратным возрастанием потребления кислорода организмом и максимальным сердечным выбросом на килограмм массы тела ребенка.
К 6-8 неделям интенсивность работы сердца значительно снижается. При расчете сердечного выброса на 1 м2 поверхности тела ударный индекс (19±5 мл/м2) и сердечный индекс (2,6+0,7 л/мин/м2) у детей первых 2 мес. достоверно ниже, чем у детей старше 2 мес. (24,5±5 мл/м2 и 3,2±0,7 л/мин/м2 в среднем, р
После рождения устанавливаются также нормальные гемодинамические режимы работы желудочков – правого, нагнетающего кровь в легочные сосуды с относительно низким сопротивлением, и левого, нагнетающего кровь в большой круг кровообращения с высоким сосудистым сопротивлением, что сказывается на отношении времени ускорения (ВУ) и времени изгнания (ВИ) желудочков

Окончательные формальные параметры работы правого и левого отделов сердца приведены на рисунке. В норме реальное давление в правом желудочке и легочной артерии составляет 20-30% от системного давления, насыщение в правых отделах сердца колеблется от 65 до 80%, в левых – от 95 до 98%. У новорожденных или седатированных детей оно может быть ниже.
Перестройка кровообращения влияет на морфологические характеристики правого и левого желудочков, которые претерпевают различную трансформацию. К концу первого года жизни толщина стенки левого желудочка становится почти в два раза больше, чем правого, а его полость практически не изменяется (рис. 1-9). Для правого желудочка динамика этих показателей противоположная: толщина стенки по сравнению с моментом рождения остается прежней, а полость увеличивается вдвое.
Общее легочное сопротивление у новорожденного.
Общее легочное сопротивление у новорожденного (ОЛС) в первые 24 часа после рождения уменьшается на -70% по сравнению с исходным, однако давление в легочной артерии все еще остается на уровне 60-85% от системного. Постепенная его нормализация происходит к 14 суткам, а может затягиваться и до 1,5 мес. Что касается морфологической постнатальной перестройки легочных сосудов, то она заканчивается к 2-3 месяцам.
В процессе быстрого снижения ОЛС важную роль играют кислород и ряд вазоактивных субстанций, вырабатываемых в процессе родов. В экспериментах на животных доказано, что низкое р02 в легочной артерии во внутриутробном периоде поддерживает констрикцию легочных сосудов и низкий кровоток, а его повышение сопровождается увеличением легочного кровотока. На резистентность легочных сосудов влияют также продукты метаболизма арахидоновой кислоты, наиболее важными из которых являются простагландины (PGE, PGD) и простациклин (PGI2).
К повышению продукции последнего приводят растяжение легких или их механическая стимуляция, действие брадикинина и ангиотензина-П. Кроме того, происходит дегрануляция тучных клеток, высвобождающих гистамин и PGD, которые у новорожденных вызывают снижение давления и сопротивления в легочных сосудах. Интересно, что гистамин и PGD в последующем действуют иначе и у взрослых вызывают вазоконстрикцию.
Помимо функциональной релаксации стенки легочных сосудов происходят и ее структурные изменения. Уменьшение резистентности легких вследствие физиологического утончения медиального слоя легочных артериол продолжается вплоть до 8 недель жизни. Процесс снижения ОЛС может длиться и в последующие годы за счет увеличения количества функционирующих легочных альвеол и связанных с ними сосудов.
– Также рекомендуем “Функция открытого овального окна. Функция открытого артериального протока.”
Оглавление темы “Основы кардиологии.”:
1. Атрезия и гипоплазия. Объем циркулирующей крови. Объем кровотока и величина шунта.
2. Общее легочное сопротивление. Сердечный выброс. Систолическая сердечная недостаточность.
3. Диастолическая сердечная недостаточность. Гипоксия и ишемия.
4. Дуктус-зависимое кровообращение. Критический порок сердца.
5. Классификация врожденных пороков сердца у новорожденных и грудных детей.
6. Сердечно-сосудистая система плода и новорожденного.
7. Особенности роста и гипертрофии миокарда новорожденных.
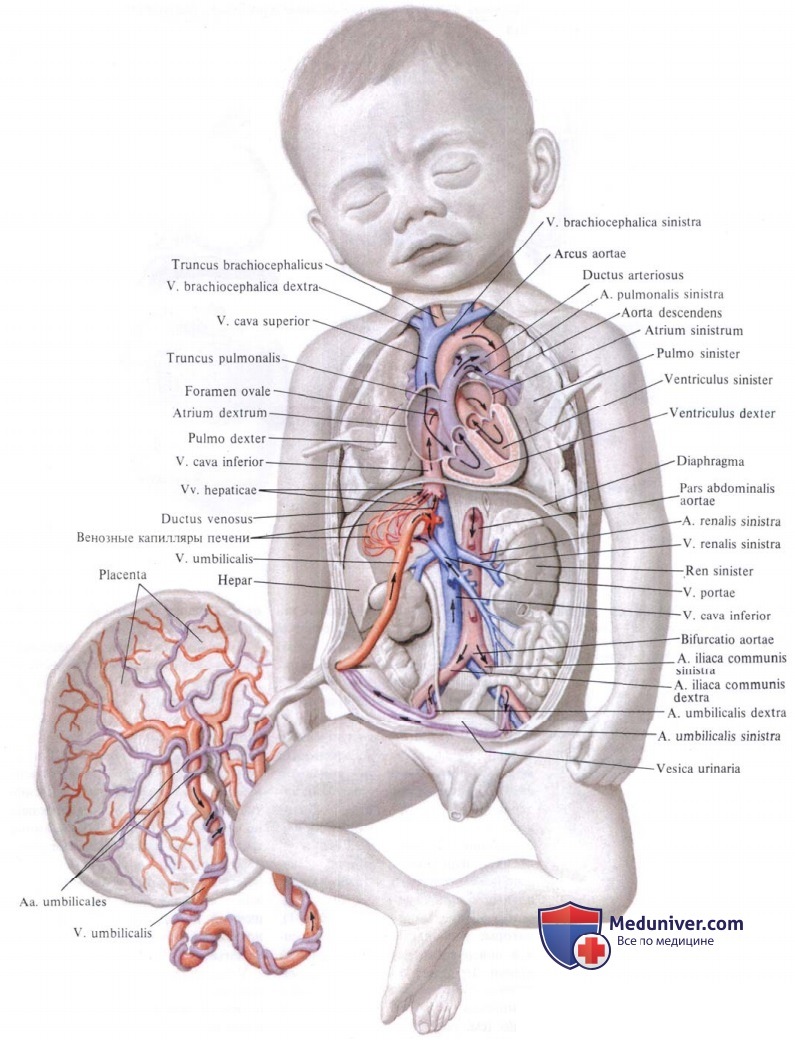
8. Кровообращение плода. Как течет кровь у плода?
9. Кровообращение новорожденного. Как течет кровь у новорожденного?
10. Функция открытого овального окна. Функция открытого артериального протока.
Источник
Фетальное кровообращение у новорожденных. Перестройка кровообращения после рождения плода.
Фетальное кровообращение у новорожденных детей частично функционирует в течение 10-15 ч внеутробной жизни. В это время сохраняется небольшой кровоток через овальное окно и артериальный проток. Возможен и двухсторонний шунт с током крови справа-налево и слева-направо. Установлено, что в первые 4 ч после рождения у большинства детей двухстороннее шунтирование крови через артериальный проток имеет несколько вариантов:
1) право-левый шунт в систолу и лево-правый шунт в диастолу;
2) право-левый шунт в систолу и двухсторонний шунт в диастолу;
3) непрерывный двухсторонний шунт в систолу и диастолу.
Право-левый ток крови обычно регистрируется в раннюю систолу, лево-правый ток крови, наблюдающийся в диастолу, продолжается длительно в течение всей диастолы. Двухсторонний турбулентный кровоток через артериальный проток имеет высокую скорость и продолжительность. С возрастанием скорости кровотока по артериальному протоку в диастолу двухсторонний шунт сменяется на лево-правый. Скорость лево-правого шунта в диастолу возрастает в первые 12 ч после рождения ребенка.
Частично циркулирующие фетальные коммуникации у новорожденного ребенка играют регуляторную роль, снижая гемодинамическую нагрузку на миокард ПЖ во время послеродовой сердечно-легочной адаптации.
После рождения ребенка происходят изменения и в системе общего кровообращения. Плацентарный артериальный кровоток прекращается в течение 45-60 с после рождения. Скорость плацентарного венозного кровотока составляет 75 мл/кг-мин, замедляется через 2 мин после рождения, почти полностью прекращается на 3-й и заканчивается на 5-й минуте жизни.
Перестройка кровообращения приводит к возрастанию выброса ЛЖ примерно на 25%. В первые 2 ч после рождения резистентность периферических регуляторных сосудов низкая, в последующее время она повышается, обеспечивая таким образом необходимый уровень АД крови. В первые сутки после рождения у здоровых доношенных новорожденных наблюдается гиперкинетический тип сокращения межжелудочковой перегородки, который регистрируется до конца первой недели жизни. Такой тип сокращения межжелудочковой перегородки с высоким давлением крови в легочной артерии при транзиторной легочной гипертензии служит для облегчения работы миокарда ЛЖ. После закрытия артериального протока ударный объем ЛЖ в среднем равняется 4,0 мл, а скорость кровотока в общей системе циркуляции составляет 2,3-3,1 л/мин*м2.
Перестройка общего кровообращения сопровождается улучшением оксигенации крови и выделения углекислого газа из организма ребенка. Так, парциальное напряжение кислорода в крови в первые 10 мин жизни равняется 30 мм рт. ст., в последующие 15 мин возрастает до 60 мм рт. ст., в течение 1-го часа – до 80 мм рт. ст. и к концу первых суток жизни устанавливается на уровне 90 мм рт. ст. Парциальное напряжение углекислого газа в крови при рождении высокое (60 мм рт. ст.) и достигает уровня взрослого в течение 2-го часа жизни.
С первых по пятые сутки жизни отмечается нарастание минутного объема кровообращения, с максимальным подъемом на 3-й день после рождения. Увеличение минутного объема кровообращения происходит в значительной мере за счет возрастания ударного объема ЛЖ. Возрастание минутного объема кровообращения вместе с нормализацией общего периферического сопротивления сосудов в конечном итоге приводит к улучшению периферической циркуляции крови, увеличению кровенаполнения периферических сосудов, улучшению оттока крови из тканей и возрастанию скорости кровотока по сосудам.
После рождения постепенно повышается АД крови, особенно максимальное. Системное АД после рождения составляет в среднем 72/47 мм рт. ст., со 2-3-го дня жизни возрастает в среднем до 94/72 мм рт. ст. с наиболее значительным подъемом на 4-5-й день жизни. Возрастание системного АД связано с увеличением не только сердечного выброса, но и общего сосудистого периферического сопротивления, что обусловлено увеличением относительной массы мышечной стенки сосудистого ложа и повышением тонуса сфинктеров периферических регуляторных сосудов.
После рождения имеется устойчивая тенденция к снижению гематокрита, что также влияет на состояние общего кровотока: с уменьшением гематокрита снижается вязкость крови и возрастает скорость кровотока в общем сосудистом русле.
Метаболизм миокарда новорожденных постепенно переходит от утилизации глюкозы как основного источника энергии к потреблению жирных кислот.
Функциональное закрытие венозного протока происходит в течение первых нескольких минут жизни, а полное анатомическое закрытие – на 2-3-й неделе после рождения.
На качестве переходного кровообращения сказывается такой фактор, как время перевязки пуповины. При поздней перевязке пуповины (наложение скобок более чем через 3 мин после рождения плода) происходит возрастание объема циркулирующей крови до 60%. Этот дополнительный объем крови обеспечивает увеличение объема крови в правом и левом предсердиях («плюс-объем»), обусловливая более высокий уровень среднего АД. Среднее давление крови в предсердиях достигает исходного уровня только спустя 2-3 ч. В этом случае на сердце новорожденного ребенка падает дополнительная работа по перекачиванию большего объема крови. Кроме того, при позднем наложении скобок на пуповину происходит увеличение массы эритроцитов на 40-50%, что способствует повышению вязкости крови и, соответственно, гемодинамической нагрузки на сердце ребенка.
Переходная циркуляция сопровождается такими клиническими проявлениями, как акроцианоз, периоральный цианоз, усиливающийся при беспокойстве или крике ребенка, сердечные шумы. В первые несколько часов жизни шумы переходного кровообращения над областью сердца выслушиваются у 85% новорожденных детей. Чаще всего они обусловлены временным функционированием артериального протока с лево-правым шунтированием крови или турбулентным движением потока крови на изгибах крупных кровеносных сосудов. Отдельные сердечные шумы выслушиваются в раннюю или позднюю систолу. В первые полчаса-час после рождения на ЭКГ могут регистрироваться удлинение интервалов P-R, QRS, инверсия зубца Т в отведении VI, который в это время становится положительным за счет систолической перегрузки ПЖ.
Учебное видео анатомия кровообращения у плода
При проблемах с просмотром скачайте видео со страницы Здесь
– Также рекомендуем “Кровообращение в периоде новорожденности.”
Оглавление темы “Кровообращение у плода и новорожденного.”:
1. Особенности сердца плода и новорожденного ребенка.
2. Структурные и биохимические особенности сердца плода и новорожденного.
3. Кровообращение плода. Чем отличается кровообращение плода?
4. Переходное кровообращение плода. Особенности переходного кровообращения.
5. Закрытие артериального протока. Преждевременное закрытие артериального протока.
6. Фетальное кровообращение у новорожденных. Перестройка кровообращения после рождения плода.
7. Кровообращение в периоде новорожденности.
8. Кровообращение недоношенного ребенка. Сердце недоношенного ребенка.
9. Электрокардиография (ЭКГ). Особенности регистрации ЭКГ у новорожденных.
10. Особенности ЭКГ здоровых новорожденных. ЭКГ новорожденного в первые 2 дня жизни.
Источник

Инфузионная терапия является одним из основных способов проведения интенсивной терапии, направленной на коррекцию, поддержание и профилактику нарушений жизненных функций организма. Традиционно инфузионная терапия проводится способом внутривенного вливания лекарственных препаратов. Умение обеспечить венозный доступ является одним из главных практических навыков, определяющих высокий класс медицинского специалиста.
Если обратиться к истории, то можно узнать о применявшихся ранее внутримышечных, подкожных, внутриполостных и ректальных вливаниях. Однако эффективность этих методов оказалась сомнительной и в настоящее время они не применяются. Тяжелые осложнения, вызываемые внутриартериальным введением инфузионных препаратов, также послужил причиной отказа от применения данной методики. В настоящее время пункция и катетеризация артерий применяется, исключительно, с диагностической целью. Внутрикостные инфузии используются лишь в экстренных случаях, когда затруднен доступ к сосудистому руслу.
Методики обеспечения венозного доступа и способы проведения инфузионной терапии у новорожденных имеют свою историю.
Прогресс неонатологии, постоянное уменьшение критического гестационного возраста и веса для выхаживания новорожденных детей диктуют специалистам и производителям медицинского оборудования осваивать новые технологии и постоянно совершенствовать старые, используя современные технику и материалы.
Современные сосудистые катетеры могут быть венозными (для центральных и периферических вен) и артериальными. Могут иметь различные приспособления для фиксации, дополнительный порт для болюсного введения препаратов, камеру обратного тока, антивозвратный клапан.
Для изготовления катетеров используются материалы, характеризующиеся разными свойствами.
| МАТЕРИАЛ | ХАРАКТЕРИСТИКИ |
| Полиэтилен | Высокая степень прочности. Жесткий. Прочный. |
| Флюорополимер (тефлон) | Достаточно жесткий. Устойчив к воздействию различных химических веществ. |
| Поливинилхлорид (пвх) | Термопластичный: жесткий при комнатной температуре, более гибкий при температуре тела. |
| Силикон | Высокая степень биосовместимости, тромборезистентности. Мягкий и гибкий. Низкий риск перфорации сосуда. |
| Полиуретан | Высокая степень биосовместимости, достаточная жесткость при натяжении, износоустойчивость, тромборезистентность. Термопластичность. |
Определение размеров сосудистых катетеров основано на системе, называемой «Бирмингемский калибр проводов (Birmingham Wire Gauge)» и использует следующую логику: чем больше калибр, тем тоньше игла. Калибр определяет, сколько канюль помещается в трубку с внутренним диаметром 1″ (1 дюйм = 25,4 мм). Применение этой системы было предложено AAMI (Ассоциация по усовершенствованию медицинского инструментария США).
| Gauge | Charriere (Ch) French (Fr) | Цвет |
| 14G | 6 | |
| 16G | 5 | |
| 17G | 4,5 | |
| 18G | 4 | |
| 20G | 3 | |
| 22G | 2,5 | |
| 24G | 2 | |
| 26G |

Существуют три основных способа обеспечения венозного доступа: венепункция, венесекция и катетеризация вены. По расположению дистального участка катетера доступы могут быть периферические и центральные.
При венесекции доступ к вене осуществляется хирургическим путем. После выделения вены, как правило, на сосуд накладывается лигатура, вена пересекается и в вышележащий отрезок вводится катетер по проводнику. Если вена не пересекается, то на введенный катетер накладывается лигатура для плотного закрепления его в сосуде и гемостаза. Таким образом, в результате данного способа катетеризации сосуда, последний «выключается» из кровоснабжения и кровоток в бассейне оперированной вены в последующим зависит от развития коллатералей. Но, как известно, чем меньше гестационный возраст ребенка, тем хуже у него развита система коллатерального кровоснабжения. Метод трудоемкий, технически сложный, требует медикаментозного обезболивания. Инвазивность метода, несоответствие диаметров катетеров и вен часто приводят к развитию контактных (асептических) флебитов, что значительно укорачивает сроки использования сосудов.
Не утрачивает своего значения в неонатологии пункционный способ венозного доступа с помощью иглы-бабочки. Этот способ применяется для внутривенного болюсного введения лекарственных препаратов и кратковременной инфузионной терапии. Для пункционного венозного доступа традиционно используются вены волосистой части головы. Здесь игла легко фиксируется, но данный венозный доступ ограничивает движения ребенка, делает невозможным грудное вскармливание.
Наиболее популярным периферическим доступом в неонатальной интенсивной терапии является катетеризация периферической вены катетером на игле.
Для катетеризации выбираются следующие вены:
Тыл кисти – тыльное венозное сплетение.
Предплечье – средняя вена предплечья, добавочная латеральная вена предплечья.
Вены волосистой части головы – надблоковая, поверхностная височная, позадиушная.
Стопа – тыльное венозное сплетение.
Локтевая ямка – медиальная вена предплечья или срединная локтевая вена.
Область голеностопного сустава – малая или большая подкожная вена ноги.

В представленном списке сосуды располагаются по мере убывания предпочтения выбора. Рекомендуется избегать вен в проекции суставов, т.к. подвижность укорачивает срок использования катетера и только в случае острой необходимости использовать вены нижних конечностей, т.к. описаны случаи ишемия или гангрена нижней конечности, осложняющие инфузию в большую подкожную вену нижней конечности; механизм неясен.
Продолжительность использования периферического катетера 3-7 дней. Несмотря на то, что материалы, из которых изготовлены катетеры являются нетромбогенными, использование гепарина в дозе 0,25-0,5 Ед/мл раствора позволяет увеличивать сроки стояния катетера. Катетеры можно использовать для прерывистой инфузии. Они не ограничивают подвижности ребенка. Недостатком периферических катетеров является невозможность длительного использования их (не более 2-3 часов) для введения вазоактивных и гиперосмолярных растворов, к которым относятся все кардиотонические препараты (допамин, добутамин, адреналин) и концентрированные растворы глюкозы, жиров, и амнокислот для парентерального питания.
Потенциальные осложнения: боль, асептические и инфекционные флебиты, экстравазация, артериоспазм (некроз). Избежать подобных осложнений возможно при правильном выборе катетера соответствующего диаметра, четкости выполнения протокола постановки катетера, строгом соблюдении правил асептики, как при катетеризации, так и при уходе за функционирующим катетером.
Катетеризация центральных вен. По определению считается, что катетер установлен в центральную позицию в том случае, когда его дистальный отрезок находится в верхней или нижней полой вене. Иными словами, в организме человека существуют только две центральные вены – верхняя и нижняя полые вены, все остальные периферические и катетеры, установленные в них должны использоваться по правилам периферических катетеров.
Показания к центральному венозному доступу
a) Полное парентеральное питание;
b) Длительная необходимость внутривенного введения лекарственных средств;
c) Внутривенное назначение гиперосмолярных растворов или раздражающих стенку сосудов лекарственных средств, которые нельзя вводить через периферические внутривенные катетеры (дофамин, добутамин, адреналин, норадреналин, растворы глюкозы в концентрации выше 12,5%, растворы АМКТ в концентрации более 2%, растворы жировых эмульсий в концентрации более 10%);
d) Интенсивная инфузионная терапия.
Противопоказания к центральному венозному доступу
Абсолютных противопоказаний не существует.
a) Инфекционное поражение кожи в месте введения катетера.
b) Возможность адекватного лечения пациента с помощью периферического венозного доступа.
Центральный венозный катетер может быть установлен путем пункции вены и катетеризации по методу Сельдингера (Seldinger), путем катетеризации через периферическую вену, хирургическим путем.
Катетеризация методом Сельдингера предусматривает пункцию вены «вслепую», по топографии с последующим введением катетера по проводнику. Этот метод сопряжен с высоким риском травматизации близлежащих жизненно важных органов, сосудов и нервных стволов, поэтому использование этого венозного доступа требует большого практического опыта врача и адекватного общего обезболивания пациента.
Особый вид катетеризации центральной вены у новорожденных детей – катетеризация пупочной вены. Это быстрый и надежный центральный доступ, позволяющий проводить интенсивную терапию с момента рождения ребенка и далее в течение двух-трех суток. Пупочные катетеры используются для проведения операций заменного переливания крови при гемолитической болезни новорожденного. У детей с экстремально низкой массой тела при рождении (ЭНМТ) пупочные катетеры иногда становятся единственным возможным сосудистым доступом и могут использоваться 2-3 недели, что требует неукоснительного соблюдения правил асептики при постановке катетера и проведении ИТ.
Самым популярным способом катетеризации центральных вен у новорожденных детей в настоящее время является установка глубоких венозных линий через периферические вены (ЦПВК). Удобство в использовании, возможность длительного применения сделали ЦПВК незаменимыми в неонатологической практике, особенно при выхаживании детей с ЭНМТ.

Места введения
1. Вены кубитальной ямки: медиальная и латеральная подкожные вены руки.
2. Вены волосистой части головы: височная и задняя ушная вена.
3. Подкожные вены ноги.
4. Подмышечная вена.
5. Наружная яремная вена.
Предпочтение отдается медиальным подкожным венам и венам правой руки, поскольку они короче и идут более прямо по направлению к центральной вене. Катетер труднее провести через латеральную подкожную вену руки из-за сужения сосуда при вхождении в дельтовидно-грудную борозду и впадения в подключичную вену под острым углом. Подмышечную и наружную яремную вену следует выбирать для введения катетера в последнюю очередь, т.к. эти вены прилежат к артериям и нервам.
При катетеризации вен бассейна верхней полой вены (ВПВ) дистальный конец катетера должен располагаться в ВПВ, на границе впадения ее в правое предсердие (ориентировочно третье межреберье справа).
При катетеризации вен бассейна нижней полой вены (НПВ) дистальный конец катетера должен располагаться в НПВ на границе впадения ее в правое предсердие (мечевидный отросток грудины).
Осложнения катетеризации.
1. Повреждение других сосудов и органов во время установки катетера: кровотечение, пункция артерии, повреждение плечевого сплетения.
2. Флебит.
3. Миграция и неправильное положение катетера. Может происходить во время установки катетера или из-за спонтанной миграции в любой момент пребывания в вене. Это может стать источником формирования тромбов на катетере и развития тромбоэмболии. Следует помнить о возможности развития «парадоксальная эмболия», обусловленной фетальными сосудистыми и внутрисердечными коммуникациями.
4. Катетер-ассоциированные инфекции кровотока. Бактерии могут колонизировать наружную поверхность катетера и затем мигрировать по ней из пространства между катетером и кожей к внутрисосудистому концу катетера. Или в результате колонизации коннектора, инфузионных сред может происходить миграция бактерий по внутренней поверхности катетера и попадание возбудителя непосредственно в кровоток.
Методы профилактики осложнений при катетеризации центральных вен:
– выполнение катетеризации только опытными специалистами;
– необходимость получения информированного согласия родителей перед процедурой;
– строгое соблюдение инструкции производителя по использованию катетера;
– обязательность подтверждения положения внутрисосудистого конца катетера рентгенологически;
– строгое соблюдение правил инфекционной безопасности сотрудниками отделений реанимации и интенсивной терапии, приходящими в отделение специалистами-консультантами и родителями;
– применение гепарина в дозе 0,5-1,0 МЕ/мл инфузионного раствора статистически не изменяет частоту возникновения тромбозов, но значительно увеличивает сроки использования катетеров;
– по возможности, не использовать катетер для парентерального питания в иных целях;
– максимальное уменьшение количества манипуляций с катетером;
– ограничение использования запорных кранов, увеличивающих риск развития инфекционных осложнений;
– удаление центрального катетера при отсутствии необходимости в нём!
Катетеризация сосудов в неонатологической практике – это искусство, требующее постоянного совершенствования навыков и современных знаний физиологии и патологии новорожденного ребенка.
Источник
