Врожденные пороки крупных сосудов
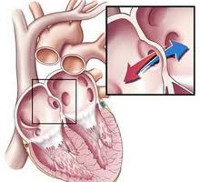
Врожденные пороки сердца и крупных сосудов возникают вследствие нарушений нормального формирования сердца в процессе эмбриогенеза.
Точный учет распространенности врожденных пороков сердца, по-видимому, провести трудно. Это объясняется тем, что врожденные пороки сердца отличаются большим разнообразием клинических проявлений. Согласно статистическим данным, на каждые 1000 родов рождается от 1 до 8 детей с пороком сердца. В течение первого года жизни погибает 54,4% детей, к 5 годам — 84,4% и только 20% детей с врожденными пороками сердца доживают до более старшего возраста.
Этиология и патогенез. В настоящее время считают, что универсальной причины, вызывающей развитие врожденных пороков сердца, не существует. Решающим является не причина, а период беременности, в котором она оказала свое действие. Наибольшая опасность для нарушения эмбриогенеза существует в течение первых трех месяцев беременности (критический период), когда формируется сердце и крупные сосуды. Большое значение имеют вирусные заболевания, перенесенные в этот период. Роль наследственности в возникновении пороков сердца до настоящего времени остается дискуссионной. В последние годы получила распространение теория о том, что врожденные заболевания могут передаваться по принципу «от органа к органу». В работах многих авторов отмечено отрицательное влияние тяжелых пороков сердца матери на развитие плода.
Эмбриогенез. В результате нарушений процесса нормального эмбриогенеза может сформироваться изолированный или комбинированный порок сердца.
Наиболее частая аномалия межпредсердной перегородки — открытое овальное отверстие, что является результатом несращения свободных сегментов клапанов овального окна.
На 4-й неделе внутриутробного развития в верхнезадней части внутренней поверхности общего предсердия образуется выступ, растущий в виде серповидной складки — первичная перегородка, эта перегородка разделяет общее предсердие на правую и левую половины. В ней образуется так называемое первичное овальное отверстие, через которое часть крови из правого предсердия переходит в левое. (Если отверстие остается после рождения, возникает первичный дефект межпредсердной перегородки).
Позднее рядом (немного правее) с первичной межпредсердной перегородкой образуется вторичная перегородка. Имеющееся в ней отверстие, так называемое вторичное овальное отверстие, которое лежит несколько сзади от первичного отверстия, прикрывается первичной перегородкой. При внутриутробном развитии давление крови в левом предсердии невелико, и вторичное отверстие остается открытым. С момента рождения ребенка, с началом легочного дыхания давление в левом предсердии повышается, и первичная перегородка предсердия, играющая роль клапана овального отверстия, закрывает последнее. Если отверстие не прикрывается — возникает вторичный дефект межпредсердной перегородки.
Дефекты межжелудочковой перегородки чаще всего возникают в ее перепончатой части, которая является остатком перегородки артериального ствола. Из артериального ствола формируется аорта и легочной ствол.
При нарушении процесса разделения артериального ствола (на 6-й неделе развития) возникает узкий легочный ствол и широкая аорта. Стеноз легочной артерии почти неизменно приводит к дефекту межжелудочковой перегородки. Аорта из-за своей ненормальной ширины смещается вправо и оказывается расположенной над межжелудочковым дефектом. Такое сочетание сопровождается гипертрофией правого желудочка и называется тетрадой Фалло.
Классификация. Разнообразие анатомических вариантов врожденных пороков сердца привело к созданию большого числа классификаций. В клинической практике все врожденные пороки разделяют на «синие» и «белые». Р. Хегглин предлагает разделять их на 3 группы:1) пороки без цианоза (стеноз устья аорты, изолированная коарктация аорты и др.);
2) пороки с ранним цианозом (триада и тетрада Фалло);
3) пороки с обязательным или необязательным поздним цианозом (дефекты межпредсердной и межжелудочковой перегородки, открытый артериальный проток).
В настоящее время наибольшее распространение получила классификация, согласно которой все врожденные пороки сердца делятся на 3 группы в зависимости от состояния легочного кровотока:
I группа — пороки с увеличенным легочным кровотоком (дефекты перегородок, открытый артериальный проток);
II группа — пороки с неизмененным легочным кровотоком (стеноз устья аорты и коарктация аорты);
III группа — пороки с уменьшенным легочным кровотоком (изолированный стеноз легочной артерии, триада и тетрада Фалло).
Общая симптоматология. Клиническая картина врожденных пороков сердца полиморфна и определяется анатомией порока, степенью нарушения гемодинамики, адаптационно-компенсаторных механизмов, характером осложнений. Многие симптомы присущи большинству пороков и на основании их можно заподозрить или диагностировать врожденную аномалию сердца. Однако ряд анома лий сердца у новорожденных и у детей раннего возраста имеют скудную симптоматику, и часто диагноз можно поставить только при тщательном обследовании.
Дети, страдающие врожденными пороками сердца со значительными нарушениями гемодинамики, отстают в развитии (в весе и росте), у них позже развиваются статические и моторные функции, запаздывает прорезывание зубов, они склонны к рахиту.
Перкуторное определение границ сердца не имеет особого значения в распознавании врожденных пороков сердца. Выслушивание же часто имеет решающее значение не только в выявлении порока, но и в определении характера его. (В большинстве случаев выслушивается систолический шум).
Можно определить различную качественную характеристику пульса и различную высоту артериального давления на обеих лучевых артериях, а также на верхних и нижних конечностях, что характерно для коарктации аорты.
Набухание шейных вен в вертикальном положении больного свидетельствует о венозном застое в большом круге кровообращения, что бывает при правожелудочковой или общей недостаточности сердца.
Врожденные пороки сердца часто сопровождаются одышкой. В механизме одышки принимают участие 3 основных фактора: снижение минутного объема сердца, накопление CO2 в крови, венозный застой в легких. Одышка в связи с недостаточным насыщением артериальной крови кислородом возникает при тетраде Фалло. Причем для данного порока характерны приступы одышки, при которых ребенок принимает вынужденное положение. Одышка может возникать и при пороках с артерио-венозным шунтом (сбросом крови), механизм развития ее очень сложен.
Кожные покровы у детей с артерио-венозным шунтом обычно бледные, а у больных с венозно-артериальным шунтом — цианотичные. Видимый цианоз наблюдается при повышенной средней капиллярной ненасыщенности крови кислородом (выше 6,5 об. %, в норме — 3,5 об. %), т. е. при содержании в капиллярной крови повышенного (5 г%, в норме — 2,5 г%) количества восстановленного, не связанного с кислородом, гемоглобина.
При пороках, сопровождающихся выраженным цианозом, развивается вторичная полицитемия. Возникновение последней связывают с реакцией костного мозга на гипоксемию. Это является компенсаторным механизмом, способствующим увеличению кислородной емкости крови. Количество эритроцитов достигает 6—8, а иногда 10 млн. и больше, но параллельно увеличивается содержание гемоглобина (120 —150%), что еще больше усугубляет ненасыщенность крови кислородом.
При длительной гипоксемии происходит утолщение концевых фаланг пальцев рук и ног в виде барабанных палочек и ногти приобретают вид часовых стекол.
Выпячивание грудной клетки в области сердца (сердечный горб) свидетельствует о значительном увеличении правого желудочка. При пороках, сопровождающихся увеличением ствола легочной артерии, можно прощупать, а иногда увидеть систолическую пульсацию во II—111 межреберьях у левого края грудины (симптом Таланкина). Коллатеральная сосудистая сеть по бокам грудной клетки и в межлопаточной области наблюдается при коарктации аорты. «Кошачье мурлыканье» у левого края грудины чаще встречается при врожденных пороках сердца.
Необходимо учитывать фазовость течения врожденных пороков сердца. После рождения ребенок вступает в фазу адаптации к нарушениям гемодинамики. Она протекает тяжело и продолжается в среднем 1,5—2,5 года.По мере развития адаптационно-приспособительных механизмов наступает фаза относительной компенсации. В дальнейшем нарушения гемодинамики усугубляются и приводят к необратимым изменениям — фаза необратимой декомпенсации, или терминальная фаза.
Источник
Врожденные пороки сердца – группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции – оперативной коррекции выявленной аномалии.
Общие сведения
Врожденные пороки сердца – весьма обширная и разнородная группа заболеваний сердца и крупных сосудов, сопровождающихся изменением кровотока, перегрузкой и недостаточностью сердца. Частота встречаемости врожденных пороков сердца высока и, по оценке различных авторов, колеблется от 0,8 до 1,2% среди всех новорожденных. Врожденные пороки сердца составляют 10-30% всех врожденных аномалий. В группу врожденных пороков сердца входят как относительно легкие нарушения развития сердца и сосудов, так и тяжелые формы патологии сердца, несовместимые с жизнью.
Многие виды врожденных пороков сердца встречаются не только изолированно, но и в различных сочетаниях друг с другом, что значительно утяжеляет структуру дефекта. Примерно в трети случаев аномалии сердца сочетаются с внесердечными врожденными пороками ЦНС, опорно-двигательного аппарата, ЖКТ, мочеполовой системы и пр.
К наиболее частым вариантам врожденных пороков сердца, встречающимся в кардиологии, относятся дефекты межжелудочковой перегородки (ДМЖП – 20%), дефекты межпредсердной перегородки (ДМПП), стеноз аорты, коарктация аорты, открытый артериальный проток (ОАП), транспозиция крупных магистральных сосудов (ТКС), стеноз легочной артерии (10-15% каждый).

Врожденные пороки сердца
Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдром Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий – глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
Кроме краснухи беременной, опасность для плода в плане развития врожденных пороков сердца представляют ветряная оспа, простой герпес, аденовирусные инфекции, сывороточный гепатит, цитомегалия, микоплазмоз, токсоплазмоз, листериоз, сифилис, туберкулез и др.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
Классификация врожденных пороков сердца
Существует несколько вариантов классификаций врожденных пороков сердца, в основу которых положен принцип изменения гемодинамики. С учетом влияния порока на легочный кровоток выделяют:
- врожденные пороки сердца с неизмененным (либо незначительно измененным) кровотоком в малом круге кровообращения: атрезия аортального клапана, стеноз аорты, недостаточность легочного клапана, митральные пороки (недостаточность и стеноз клапана), коарктация аорты взрослого типа, трехпредсердное сердце и др.
- врожденные пороки сердца с увеличенным кровотоком в легких: не приводящие к развитию раннего цианоза (открытый артериальный проток, ДМПП, ДМЖП, аортолегочный свищ, коарктация аорты детского типа, синдром Лютамбаше), приводящие к развитию цианоза (атрезия трехстворчатого клапана с большим ДМЖП, открытый артериальный проток с легочной гипертензией)
- врожденные пороки сердца с обедненным кровотоком в легких: не приводящие к развитию цианоза (изолированный стеноз легочной артерии), приводящие к развитию цианоза (сложные пороки сердца – болезнь Фалло, гипоплазия правого желудочка, аномалия Эбштейна)
- комбинированные врожденные пороки сердца, при которых нарушаются анатомические взаимоотношения между крупными сосудами и различными отделами сердца: транспозиция магистральных артерий, общий артериальный ствол, аномалия Тауссиг-Бинга, отхождение аорты и легочного ствола из одного желудочка и пр.
В практической кардиологии используется деление врожденных пороков сердца на 3 группы: пороки «синего» (цианотического) типа с веноартериальным шунтом (триада Фалло, тетрада Фалло, транспозиция магистральных сосудов, атрезия трехстворчатого клапана); пороки «бледного» типа с артериовенозным сбросом (септальные дефекты, открытый артериальный проток); пороки с препятствием на пути выброса крови из желудочков (стенозы аорты и легочной артерии, коарктация аорты).
Нарушения гемодинамики при врожденных пороках сердца
В результате выше названных причин у развивающего плода может нарушаться правильное формирование структур сердца, что выражается в неполном или несвоевременном закрытии перепонок между желудочками и предсердиями, неправильном образовании клапанов, недостаточном повороте первичной сердечной трубки и недоразвитии желудочков, аномальном расположении сосудов и т. д. После рождения у части детей остаются открытыми артериальный проток и овальное окно, которые во внутриутробном периоде функционируют в физиологическом порядке.
Ввиду особенностей антенатальной гемодинамики, кровообращение развивающегося плода при врожденных пороках сердца, как правило, не страдает. Врожденные пороки сердца проявляются у детей сразу после рождения или через какое-то время, что зависит от сроков закрытия сообщения между большим и малым кругами кровообращения, выраженности легочной гипертензии, давления в системе легочной артерии, направления и объема сброса крови, индивидуальных адаптационных и компенсаторных возможностей организма ребенка. Нередко к развитию грубых нарушений гемодинамики при врожденных пороках сердца приводит респираторная инфекция или какое-либо другое заболевание.
При врожденных пороках сердца бледного типа с артериовенозным сбросом вследствие гиперволемии развивается гипертензия малого круга кровообращения; при пороках синего типа с веноартериальным шунтом у больных имеет место гипоксемия.
Около 50% детей с большим сбросом крови в малый круг кровообращения погибают без кардиохирургической помощи на первом году жизни от явлений сердечной недостаточности. У детей, перешагнувших этот критический рубеж, сброс крови в малый круг уменьшается, самочувствие стабилизируется, однако постепенно прогрессируют склеротические процессы в сосудах легких, обусловливая легочную гипертензию.
При цианотических врожденных пороках сердца венозный сброс крови или ее смешение приводит к перегрузке большого и гиповолемии малого круга кровообращения, вызывая снижение насыщения крови кислородом (гипоксемию) и появление синюшности кожи и слизистых. Для улучшения вентиляции и перфузии органов развивается коллатеральная сеть кровообращения, поэтому, несмотря на выраженные нарушения гемодинамики, состояние больного может длительное время оставаться удовлетворительным. По мере истощения компенсаторных механизмов, вследствие длительной гиперфункции миокарда, развиваются тяжелые необратимые дистрофические изменения в сердечной мышце. При цианотических врожденных пороках сердца оперативное вмешательство показано уже в раннем детском возрасте.
Симптомы врожденных пороков сердца
Клинические проявления и течение врожденных пороков сердца определяется видом аномалии, характером нарушений гемодинамики и сроками развития декомпенсации кровообращения.
У новорожденных с цианотическими врожденными пороками сердца отмечается цианоз (синюшность) кожных покровов и слизистых оболочек. Синюшность усиливается при малейшем напряжении: сосании, плаче ребенка. Белые пороки сердца проявляются побледнением кожи, похолоданием конечностей.
Дети с врожденными пороками сердца обычно беспокойные, отказываются от груди, быстро устают в процессе кормления. У них появляется потливость, тахикардия, аритмии, одышка, набухание и пульсация сосудов шеи. При хроническом нарушении кровообращения дети отстают в прибавлении веса, росте и физическом развитии. При врожденных пороках сердца обычно сразу поле рождения выслушиваются сердечные шумы. В дальнейшем обнаруживаются признаки сердечной недостаточности (отеки, кардиомегалия, кардиогенная гипотрофия, гепатомегалия и др.).
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит, полицитемия, тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии, синкопальные состояния, одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда.
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой – электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки, эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург.
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки, рентгенэндоваскулярную окклюзию дефекта. При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство, предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена, Сеннинга, Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы, отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ, биопсия хориона, амниоцентез) и показаниях к прерыванию беременности. Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
Источник
