В закрытом сосуде находятся водород и азот
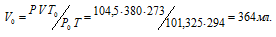
В
условиях задач этого раздела температура задается в градусах Цельсия.
При проведении числовых расчетов необходимо перевести температуру в
градусы Кельвина, исходя из того, что 0° С = 273° К. Кроме того,
необходимо также представить все остальные величины в единицах системы
СИ. Так, например, 1л = 10-3 м3; 1м3 = 106 см3 = 109 мм3.Если
в задаче приведена графическая зависимость нескольких величин от
какой-либо одной и при этом все кривые изображены на одном графике, то
по оси у задаются условные единицы. При решении задач используются данные таблиц 3,6 и таблиц 9—11 из приложения.
5.1. Какую температуру T имеет масса m = 2 г азота, занимающего объем V = 820 см3 при давлении p = 0,2 МПа?
5.2. Какой объем V занимает масса m = 10г кислорода при давлении р = 100 кПа и температуре t = 20° С?
5.3. Баллон объемом V = 12 л наполнен азотом при давлении p = 8,1МПа и температуре t = 17° С. Какая масса m азота находится в баллоне?
5.4. Давление воздуха внутри плотно закупоренной бутылки при температуре t1=7C было p1= 100 кПа. При нагревании бутылки пробка вылетела. До какой температуры t2нагрели бутылку, если известно, что пробка вылетела при давлении воздуха в бутылке p = 130 кПа?
5.5. Каким должен быть наименьшей объем V баллона, вмещающего массу m = 6,4 кг кислорода, если его стенки при температуре t = 20° С выдерживают давление p = 15,7 МПа?
5.7. Найти массу m сернистого газа (S02), занимающего
объем V = 25 л при температуре t=27С и давлении p = 100 кПа.
5.6. В баллоне находилась масса m1= 10 кг газа при давлении p1 = 10 МПа. Какую массу Am газа взяли из баллона, если давление стало равным p2= 2,5 МПа? Температуру газа считать постоянной.
5.8. Найти массу m воздуха, заполняющего аудиторию высотой h = 5 м и площадью пола S = 200 м2. Давление воздуха p = 100кПа, температура помещения t = 17° С. Молярная масса воздуха u = 0,029 кг/моль.
5.9. Во сколько раз плотность воздуха p1, заполняющего помещение зимой (t1 =7°С), больше его плотности p2летом (t2=37° С)? Давление газа считать постоянным.
5.10. Начертить изотермы массы m = 0,5 г водорода для температур: а) t1 = 0° С; б) t2 = 100° С.
5.11. Начертить изотермы массы m = 15,5г кислорода для температур: a) t1 = 39° С; б) t2 =180° С.
5.12. Какое количество v газа находится в баллоне объемом V = 10 м3 при давлении p =96 кПа и температуре t = 17° С?
5.13. Массу m =5 г азота, находящегося, в закрытом сосуде объемом V = 4 л при температуре t1 = 20° С, нагревают до температуры t2 = 40° С. Найти давление p1 и p2газа до и после нагревания.
5.14. Посередине откачанного и запаянного с обеих концов капилляра,
расположенного горизонтально, находится столбик ртути длиной l = 20 см.
Если капилляр поставить вертикально, то столбик ртути переместится на dl
= 10 см. До какого давления p0был откачан капилляр? Длина капилляра L –1 м.
5.15. Общеизвестен шуточный вопрос: «Что тяжелее: тонна свинца или
тонна пробки?» На сколько истинный вес пробки, которая в воздухе весит
9,8кН, больше истинного веса свинца, который в воздухе весит также
9,8кН? Температура воздуха t = 17° С, давление p = 100кПа.
5.16. Каков должен быть вес p оболочки детского воздушного шарика, наполненного водородом, чтобы результирующая подъемная сила шарика F =
0 , т.е. чтобы шарик находился во взвешенном состоянии? Воздух и
водород находится при нормальных условиях. Давление внутри шарика равно
внешнему давлению. Радиус шарика r = 12,5 см.
5.17. При температуре t = 50° С давление насыщенного водяного пара p = 12,3 кПа. Найти плотность p водяного пара.
5.18. Найти плотность p водорода при температуре t = 10° С и давлении p = 97,3 кПа.
5.19. Некоторый газ при температуре t = 10° С и давлении p = 200 кПа имеет плотность p = 0,34 кг/м3. Найти молярную массу u газа.
5.20. Сосуд откачан до давления p = 1,33 • 10-9 Па; температура воздуха t = 15° С. Найти плотность p воздуха в сосуде.
5.21. Масса m = 12 г газа занимает объем V = 4 л при температуре t1 = 7° С. После нагревания газа при постоянном давлении его плотность стала равной p = 0,6 кг/м3. До какой температуры г, нагрели газ?
5.22. Масса m = 10г кислорода находится при давлении p = 304 кПа и температуре t1=10° С. После расширения вследствие нагревания при постоянном давлении кислород занял объ-
ем V2=10 л. Найти объем V1газа до расширения, температуру t2 газа после расширения, плотности p1и p2газа до и после расширения.
5.23. В запаянном сосуде находится вода, занимающая объем, равный половине объема сосуда. Найти давление p и плотность
p водяного пара при температуре t = 400° С, зная, что при этой
температуре вся вода обращается в пар.
5,24. Построить график зависимости плотности p кислорода: а) от давления p при температуре Т = const = 390 К в интервале
0 < p < 400 кПа через каждые 50 кПа; б) от температуры Т при p = const = 400 кПа в интервале 200 < Т < 300 К через каждые 20К.
5.25. В закрытом сосуде объемом V = 1 м3 находится масса m1= 1,6 кг кислорода и масса m2= 0,9 кг воды. Найти давление p в сосуде при температуре t = 500° С, зная, что при этой температуре вся вода превращается в пар.
5.26. В сосуде 1 объем V1 = 3 л находится газ под давлением p1= 0,2 МПа. В сосуде 2 объем V2 = 4 л находится тот же газ под давлением p2= 0,1 МПа. Температуры газа в обоих сосудах одинаковы. Под каким давлением p будет находиться газ, если соединить сосуды 1 и 2 трубкой?
5.27. В сосуде объемом V = 2 л находится масса m1= 6 г углекислого газа (С02) и масса m2закиси азота (N20) при температуре t = 127° С. Найти давление p смеси в сосуде.
5.28. В сосуде находится масса m1 = 14 г азота и масса m2=9гводорода при температуре t = 10°С и давлении p = 1 МПа. Найти молярную массу p смеси и объем V сосуда.
5.29. Закрытый сосуд объемом V = 2 л наполнен воздухом при нормальных условиях. В сосуд вводится диэтиловый эфир (С2Н5ОС2Ы5). После того как весь эфир испарился, давление в сосуде стало равным p = 0,14 МПа. Какая масса m эфира была введена в сосуд?
5.30. В сосуде объемом V = 0,5 л находится масса m = 1 г парообразного йода (I2). При температуре t = 1000° С давление в сосуде pс= 93,3 кПа. Найти степень диссоциации а молекул йода на атомы. Молярная масса молекул йода u = 0,254 кг/моль.
5.31. В сосуде находится углекислый газ. При некоторой температуре
степень диссоциации молекул углекислого газа на кислород и окись
углерода а = 0,25 . Во сколько раз давление в сосуде при этих
условиях будет больше того давления, которое имело бы место, если бы
молекулы углекислого газа не были диссоциированы?
5.32. В воздухе содержится 23,6% кислорода и 76,4% азота (по массе) при давлении p = 100кПа и температуре t = 13° С.
Найти плотность p воздуха и парциальные давления p1и p2
кислорода и азота.
5.33. В сосуде находится масса m1 = 10 г углекислого газа и масса m2=15г азота. Найти плотность p смеси при температуре t = 27° С и давлении p = 150 кПа.
5.34. Найти массу m0атома: а) водорода; б) гелия.
5.35. Молекула азота, летящая со скоростью v = 600 м/с, упруго ударяется о стенку сосуда по нормали к ней. Найти импульс силы Fdt, полученный стенкой сосуда за время удара.
5.36, Молекула аргона, летящая со скоростью v = 500 м/с, упруго
ударяется о стенку сосуда. Направление скорости молекулы и нормаль к
стенке сосуда составляют угол а = 60° . Найти импульс силы Fdt, полученный стенкой сосуда за время удара.
5.37. Молекула азота летит со скоростью v = 430 м/с. Найти импульс mv этой молекулы.
5.38. Какое число молекул n содержит единица массы водяного пара?
5.39. В сосуде объемом V = 4 л находится масса m = 1 г водорода. Какое число молекул n содержит единица объема сосуда?
5.40. Какое число молекул N находится в комнате объемом V = 80 m3 при температуре t = 17° С и давлении p = 100 кПа?
5.41. Какое число молекул и содержит единица объема сосуда при температуре t = 10° С и давлении p = 1,33 * 10-9 Па?
5.42. Для получения хорошего вакуума в стеклянном сосуде необходимо
подогревать стенки сосуда при откачке для удаления адсорбированного
газа. На сколько может повыситься давление в сферическом сосуде радиусом
r = 10 см, если адсорбированные молекулы перейдут со стенок в сосуд? Площадь поперечного сечения молекул s0= 10-19 м2. Температура газа в сосуде t = 300° С. Слой молекул на стенках считать мономолекулярным.
5.43. Какое число частиц находится в единице массы парообразного йода (I2), степень диссоциации которого а = 0,5 ? Молярная масса молекулярного йода u = 0,254 кг/моль.
5.44. Какое число частиц N находится в массе m = 16г кислорода, степень диссоциации которого а = 0,5 ?
5.45. В сосуде находится количество v1=10-7 молей кислорода и масса m2=10-6г азота. Температура смеси t = 100° С, давление в сосуде p = 133мПа. Найти объем V сосуда, парциальные давления p1и p2кислорода и азота и число молекул n в единице объема сосуда.
5.46. Найти среднюю квадратичную скорость молекул воздуха при температуре t = 17° С. Молярная масса воздуха u = 0,029 кг/моль.
5.48. В момент взрыва атомной бомбы развивается температура T=107 К.
Считая, что при такой температуре все молекулы полностью диссоциированы
на атомы, а атомы ионизированы, найти среднюю квадратичную скорость
sqr(v2) иона водорода.
5.47. Найти отношение средних квадратичных скоростей молекул гелия и азота при одинаковых температурах.
5.49. Найти число молекул nводорода в единице объема сосуда при давлении p = 266,6 Па, если средняя квадратичная
скорость его молекул sqr(v2)= 2,4 км/с.
5.50. Плотность некоторого газа p = 0,06 кг, средняя
квадратичная скорость его молекул sqr(v2) = 500 м/с. Найти
давление p, которое газ оказывает на стенки сосуда.
5.51. Во сколько раз средняя квадратичная скорость пылинки, взвешенной в воздухе, меньше средней квадратичной скорости
молекул воздуха? Масса пылинки /77 = 10~8г. Воздух считать однородным газом, молярная масса которого // = 0,029 кг/моль.
5.52. Найти импульс mv молекулы водорода при температуре t = 20° С. Скорость молекулы считать равной средней квадратичной скорости.
5.53. В сосуде объемом V = 2лнаходится масса m = 10 г кислорода при давлении p = 90,6 кПа. Найти среднюю
5.216. Найти изменение dS энтропии при превращении массы m = 10 г льда (t = -20° С) в пар (tn = 100° С).
5.55. Средняя квадратичная скорость молекул некоторого
газа sqr(v2) = 450 м/с. Давление газа p = 50 кПа. Найти плотность p газа при этих условиях.
5.56. Плотность некоторого газа p = 0,082 кг/м3 при давлении p = 100кПа и температуре t = 17° С. Найти среднюю квадратичную скорость sqr(v2) молекул газа. Какова молярная масса p этого газа?
5.218. Найти изменение dS энтропии при плавлении массы m = 1кг льда (t = 0° С).
5.219. Массу m = 640 г расплавленного свинца при температуре плавления tплвылили на лед (t = 0° С). Найти изменение dS энтропии при этом процессе.
5.60. Найти энергию Wврвращательного движения молекул, содержащихся в массе m = 1 кг азота при температуре t = 7° С.
5.61. Найти внутреннюю энергию W двухатомного газа, находящегося в сосуде объемом V = 2л под давлением p = 150 кПа.
5.62. Энергия поступательного движения молекул азота, находящегося в баллоне объем V = 20 л, W = 5 кДж, а средняя квадратичная скорость его молекул sqr(v2) = 2*103 м/с. Найти массу m азота в баллоне и давление /?, под которым он находится.
5.63. При какой температуре Т энергия теплового
движения атомов гелия будет достаточна для того, чтобы атомы гелия
преодолели земное тяготние и навсегда покинули земную атмосферу? Решить
аналогичную задачу для Луны.
5.64. Масса m = 1 кг двухатомного газа находится под давлением p = 80кПа и имеет плотность p = 4кг/м3. Найти
энергию теплового движения W молекул газа при этих условиях.
5.65. Какое число молекул N двухатомного газа содержит объем V = 10см3 при давлении V = 5,3 кПа и температуре
t = 27° С? Какой энергией теплового движения W обладают эти молекулы?
5.66. Найти удельную теплоемкость cкислорода для: а) V = const; б) p = const.
5.67. Найти удельную теплоемкость сp: а) хлористого водорода; б) неона; в) окиси азота; г) окиси углерода; д) паров ртути.
5.68. Найти отношение удельных теплоемкостей сp/сtдля кислорода.
5.69. Удельная теплоемкость некоторого двухатомного газа с = 14,7 кДж/(кг-К). Найти молярную массу u этого газа.
5.70. Плотность некоторого двухатомного газа при нормальных условиях p = 1,43 кг/м3. Найти удельные теплоемкости сt и
сpэтого газа.
5.71. Молярная масса некоторого газа u = 0,03 кг/моль, отношение сp/сV = 1,4 . Найти удельные теплоемкости сV и сpэтого газа.
5.72. Во сколько раз молярная теплоемкость С гремучего газа больше молярной теплоемкости С” водяного пара, получившегося при его сгорании? Задачу решить для: а) V = const б) p = const.
5.73. Найти степень диссоциации а кислорода, если его удельная теплоемкость при постоянном давлении ср= 1,05 кДж/(кг-К).
5.74. Найти удельные теплоемкости сV и сp парообразного йода (I2), если степень диссоциации его а = 0,5. Молярная масса молекулярного йода u = 0,254 кг/моль.
5.75. Найти степень диссоциация а азота, если для него отношение сp /сV = 1,47.
5.76. Найти удельную теплоемкость сpгазовой смеси, состоящей из количества v1=Зкмоль аргона и количества v2 = 3 кмоль азота.
5.77. Найти отношение сp/сV для газовой смеси, состоящей из массы m1 = 8 г гелия и массы m2 = 16 г кислорода.
5.78. Удельная теплоемкость газовой смеси, состоящей из количества v1= 1 кмоль кислорода и некоторой массы m2аргона
равна сV = 430 Дж/(кгК),. Какая масса m2аргона находится в газовой смеси?
5.79. Масса m = 10 г кислорода находится при давлении p = 0,3 МПа и температуре t = 10° С. После нагревания при
p= const газ занял объем V2 =10л. Найти количество теплоты
Q, полученное газом, и энергию теплового движения молекул
газа W до и после нагревания.
5.80. Масса m = 12 г азота находится в закрытом сосуде объемом V =2л при температуре t = 10° С. После нагревания Давление в сосуде стало равным p = 1,33 МПа. Какое количество теплоты Q сообщено газу при нагревании?
Источник
Задача 28.
При 17°С некоторое количество газа занимает объем 580 мл. Какой объем займет это же количество газа при 100°С, если давление его останется неизменным?
Решение:
По закону Гей – Люссака при постоянном давлении объём газа изменяется прямо пропорционально абсолютной температуре (Т):
V2 – искомый объём газа;
T2 – соответствующая V2 температура;
V1 – начальный объём газа при соответствующей температуре Т1.
По условию задачи V1 = 580мл; Т1 = 290К (273 + 17 = 290) и Т2 = 373К (273 + 100 = 373). Подставляя эти значения в выражение закона Гей – Люссака, получим:
Ответ: V2 = 746мл.
Задача 29.
Давление газа, занимающего объем 2,5л, равно 121,6 кПа (912мм рт. ст.). Чему будет равно давление, если, не изменяя температуры, сжать газ до объема в 1л?
Решение:
Согласно закону Бойля – Мариотта, при постоянной температуре давление, производимое данной массой газа, обратно пропорционально объёму газа:
Обозначив искомое давление газа через Р2, можно записать:
Ответ: Р2 = 304кПа (2280мм.рт.ст.).
Задача 30. На сколько градусов надо нагреть газ, находящийся в закрытом сосуде при 0 °С, чтобы давление его увеличилось вдвое?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально температуре:
По условию задачи Т1 = 0 °С + 273 = 273К; давление возросло в два раза: Р2 = 2Р1.
Подставляя эти значения в уравнение, находим:
Ответ: Газ нужно нагреть на 2730С.
Задача 31.
При 27°С и давлении 720 мм.рт. ст. объем газа равен 5л. Кой объем займет это же количество газа при 39°С и давлении 104кПа?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 5л; Т = 298К (273 + 25 = 298); Р = 720 мм.рт.ст. (5,99 кПа); Р0 = 104 кПа; Т = 312К (273 + 39 = 312); Т = 273К. Подставляя данные задачи в уравнение, получим:
Ответ: V0 = 4,8л
Задача 32.
При 7°С давление газа в закрытом сосуде равно 96,0 кПа. Каким станет давление, если охладить сосуд до —33 °С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:
Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 96,0 кПа; Т1 = 280К (273 + 7 = 280); Т2 = 240К (273 – 33 = 240). Подставляя эти значения в уравнение, получим:
Ответ: Р2 = 82,3кПа.
Задача 33.
При нормальных условиях 1г воздуха занимает объем 773 мл. Какой объем займет та же масса воздуха при 0 °С и )и давлении, равном 93,3 кПа (700мм. рт. ст.)?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V0 = 773мл; Т0 = 298К (273 + 25 = 298); Т = 273К; Р = 93,3кПа. Подставляя данные задачи и преобразуя уравнение, получим:
Ответ: V = 769, 07 мл.
Задача 34.
Давление газа в закрытом сосуде при 12°С равно 100 кПа (750мм рт. ст.). Каким станет давление газа, если нагреть сосуд до 30°С?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:
Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 100 кПа; Т1 = 285К (273 + 12 = 285); Т2 = 303К (273 + 30 = 303). Подставляя эти значения в уравнение, получим:
Ответ: Р2 = 106,3кПа.
Задача 35.
В стальном баллоне вместимостью 12л находится при 0°С кислород под давлением 15,2 МПа. Какой объем кислорода, находящегося при нормальных условиях можно получить из такого баллона?
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: V = 12л; Т = 273К (273 + 0 = 2273); Р =15,2МПа); Р0 = 101,325кПа; Т0 = 298К (273 + 25 = 298). Подставляя данные задачи в уравнение, получим:
Ответ: V0 = 1,97м3.
Задача 36.
Температура азота, находящегося в стальном баллоне под давлением 12,5 МПа, равна 17°С. Предельное давление для баллона 20,3МПа. При какой температуре давление азота достигнет предельного значения?
Решение:
При постоянном объёме давление газа изменяется прямо пропорционально абсолютной температуре:
Обозначим искомое давление через Р2, а соответствующую ему температуру через Т2. По условию задачи Р1 = 12,5МПа; Т1 = 290К (273 + 17 = 290); Р2 = 20,3МПа. Подставляя эти значения в уравнение, получим:
Ответ: Т2 = 1980С.
Задача 37.
При давлении 98,7кПа и температуре 91°С некоторое количество газа занимает объем 680 мл. Найти объем газа при нормальных условиях.
Решение:
Зависимость между объёмом газа, давлением и температурой выражается общим уравнением, объединяющим законы Гей-Люссака и Бойля-Мариотта:
где Р и V – давление и объём газа при температуре Т; Р0 и V0 – давление и объём газа при нормальных условиях. Данные задачи: Р0 = 101,325кПа; V = 680мл; Т0 = 298К (273 + 25 = 298); Т = 364К (273 + 91 = 364); Р = 98,7кПа. Подставляя данные задачи и преобразуя уравнение, получим:
<
Ответ: V0 = 542,3мл.
Задача 38.
При взаимодействии 1,28г металла с водой выделилось 380 мл водорода, измеренного при 21°С и давлении 104,5кПа (784мм рт. ст.). Найти эквивалентную массу металла.
Решение:
Находим объём выделившегося водорода при нормальных условиях, используя уравнение:
где Р и V – давление и объём газа при температуре Т = 294К (273 +21 = 294); Р0 = 101,325кПа; Т0 = 273К; Р = 104,5кПа. Подставляя данные задачи в уравнение,
получим:
Согласно закону эквивалентов, массы (объёмы) реагирующих друг с другом веществ m1 и m2 пропорциональны их эквивалентным массам (объёмам):
Мольный объём любого газа при н.у. равен 22,4л. Отсюда эквивалентный объём водорода равен 22,4 : 2 = 11,2л или 11200 мл. Тогда, используя формулу закона эквивалентов, рассчитаем эквивалентную массу металла:
Ответ: mЭ(Ме) = 39,4г/моль.
Задача 39.
Как следует изменить условия, чтобы увеличение массы данного газа не привело к возрастанию его объема: а) понизить температуру; б) увеличить давление; в) нельзя подобрать условий?
Решение:
Для характеристики газа количеством вещества (n, моль) применяется уравнение РV = nRT, или – это уравнение Клапейрона-Менделеева. Оно связывает массу (m, кг); температуру (Т, К); давление (Р, Па) и объём (V, м3) газа с молярной массой (М, кг/моль).
Тогда из уравнения Клапейрона-Менделеева объём газа можно рассчитать по выражению:
Отсюда следует, что V = const, если при увеличении массы (m) газа на некоторую величину будет соответственно уменьшена температура (T) системы на некоторое необходимое значение. Объём системы также не изменится при постоянной температуре, если при увеличении массы (m) газа на некоторую величину будет соответственно увеличено давление (P) системы на необходимую величину.
Таким образом, при увеличении массы газа объём системы не изменится, если понизить температуру системы или же увеличить давление в ней на некоторую величину.
Ответ: а); б).
Задача 40.
Какие значения температуры и давления соответствуют нормальным условиям для газов: а) t = 25 °С, Р = 760 мм. рт. ст.; б) t = 0 °С, Р = 1,013 • 105Па; в) t = 0°С, Р = 760 мм. рт. ст.?
Решение:
Состояние газа характеризуется температурой, давлением и объёмом. Если температура газа равна 0 °С (273К), а давление составляет 101325 Па (1,013 • 105) или 760 мм. рт. ст., то условия, при которых находится газ, принято считать нормальными.
Ответ: б); в).
Источник
